
用一小粒钠投入水中,实验操作和过程中不可能感知或观察到的现象是
| A.钠的熔点低 | B.钠呈银白色、硬度小 |
| C.钠有延展性,导电性好 | D.钠具有强还原性 |
 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:单选题
下列有关实验操作的叙述正确的是( )
| A.将碘水倒入分液漏斗,加适量乙醇,振荡后静置,可将碘萃取到乙醇中 |
| B.某气体能使湿润的红色石蕊试纸变蓝,该气体水溶液一定显碱性 |
| C.NaCl 溶液蒸发结晶时,蒸发皿中刚好有晶体析出时即停止加热 |
| D.向AlCl3溶液中滴加氨水,会产生白色沉淀,再加入NaHSO4溶液,沉淀不消失 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
有相同质量的两份NaHCO3粉末,第一份加入足量盐酸,笫二份先加热使其完全分解
再加足量同质量分数的盐酸,则两者所消耗的盐酸中氯化氢的质量比为
| A.2:1 | B.1:1 | C.1:2 | D.4:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关常见金属及其化合物的说法正确的是:
| A.氯化铁溶液中加入还原性铁粉无明显颜色变化 |
| B.铁与水蒸气在高温下的反应产物为Fe2O3和H2 |
| C.AlCl3与过量NaOH溶液反应生成AlO2-,则与过量NH3·H2O也生成AlO2- |
| D.常温下1 mol铜片投入含4 mol HNO3的浓硝酸中金属可完全溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
将由Mg和Al组成的一定质量的混合物投入500 mL 稀硫酸中,固体全部溶解并产生气体。待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如右图所示。则下列说法正确的是
| A.上述由Mg和Al组成的混合物的质量为8g |
| B.硫酸的物质的量浓度为1 mol·L-1 |
| C.生成的H2在标准状况下的体积为11.2L |
| D.NaOH溶液的物质的量浓度为3.75 mol·L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
Al、Fe、Cu都是重要的金属元素。下列说法正确的是
| A.三者对应的氧化物均为碱性氧化物 |
| B.三者的单质放置在空气中均只生成氧化物 |
C.制备AlCl3、Fe Cl3、CuCl2均不能采用将溶液直接蒸干的方法 Cl3、CuCl2均不能采用将溶液直接蒸干的方法 |
| D.AlCl3、FeCl3、CuCl2均可用作净水剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
将ag Mg、Al合金完全溶解在V1L、c1mol/L的盐酸溶液中,产生bgH2。再向反应后的溶液中加入V2L,c2mol/LNaOH溶液,恰好使沉淀达到最大值,且沉淀质量为dg。则下列关系式错误的是( )
| A.合金中的物质的量为(24b-a)/9mol |
| B.d=a+17b |
C.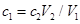 |
D.与金属反应后剩余盐酸的物质的量浓度为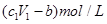 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(12分)烟气脱硫能有效减少二氧化硫的排放。实验室用粉煤灰(主要含Al2O3、SiO2等)制备碱式硫酸铝[Al2(SO4)x(OH)6—2x]溶液,并用于烟气脱硫研究。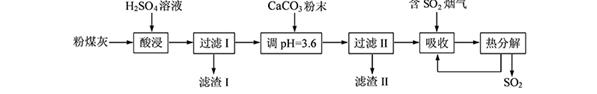
(1)酸浸时反应的化学方程式为 ;滤渣Ⅰ的主要成分为 (填化学式)。
(2)加CaCO3调节溶液的pH至3.6,其目的是中和溶液中的酸,并使Al2(SO4)3转化为Al2(SO4)x(OH)6—2x。滤渣Ⅱ的主要成分为 (填化学式);若溶液的pH偏高,将会导致溶液中铝元素的含量降低,其原因是 (用离子方程式表示)。
(3)上述流程中经完全热分解放出的SO2量总是小于吸收的SO2量,其主要原因是 ;与吸收SO2前的溶液相比,热分解后循环利用的溶液的pH将 (填“增大”、“减小”或“不变”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com