
将一质量分数为ω的KOH溶液蒸发掉m g水后,质量分数恰好变为3ω,体积为VL(溶液中无晶体析出),则浓缩后溶液的物质的量浓度为( )
A. mol·L-1 B.
mol·L-1 B.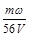 mol·L-1 C.
mol·L-1 C. mol·L-1 D.
mol·L-1 D. mol·L-1
mol·L-1
科目:高中化学 来源: 题型:
 对金属表面进行处理,形成一层致密的氧化物保护膜,是非常有效的一种金属防腐技术.
对金属表面进行处理,形成一层致密的氧化物保护膜,是非常有效的一种金属防腐技术.查看答案和解析>>
科目:高中化学 来源: 题型:
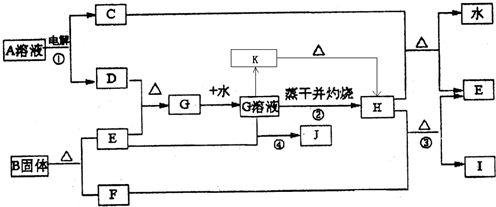
| ||
| ||
 到
到| 162.5Vc |
| m |
| 162.5Vc |
| m |
查看答案和解析>>
科目:高中化学 来源: 题型:
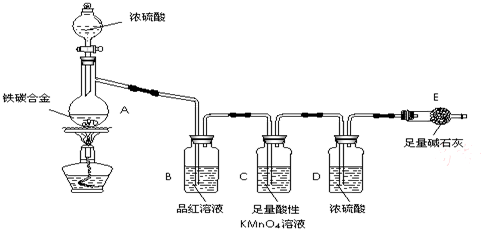
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
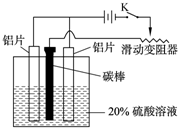
查看答案和解析>>
科目:高中化学 来源:2010年山东省济宁二中高考化学一模试卷(解析版) 题型:解答题
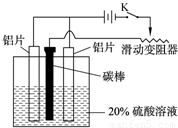
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com