
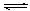 SO3��g������H=" ��98" kJ�� mol��1����ʼʱ��10L���ܱ������м���4.0mol SO2(g)��5.0molO2(g)������Ӧ�ﵽƽ��ʱ���ų�����196kJ�����¶���ƽ�ⳣ��K= ��
SO3��g������H=" ��98" kJ�� mol��1����ʼʱ��10L���ܱ������м���4.0mol SO2(g)��5.0molO2(g)������Ӧ�ﵽƽ��ʱ���ų�����196kJ�����¶���ƽ�ⳣ��K= ��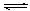 2SO3��g���ﵽƽ���ı���������SO3�����������������
2SO3��g���ﵽƽ���ı���������SO3����������������� 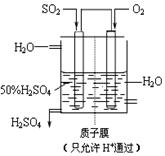

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
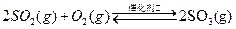

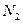 ��
�� �����
����� ,
,
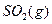 ������
������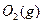 ��ַ�Ӧ����
��ַ�Ӧ����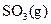 ���ų�����
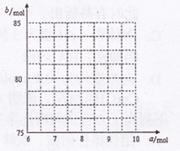
���ų����� 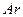 b����ƽ�������г���
b����ƽ�������г���
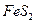 ��ȫ����
��ȫ����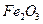 ������ʱҪʹ�ù�����
������ʱҪʹ�ù�����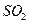 ��
��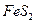 �ڿ�������ȫ���գ����ù���
�ڿ�������ȫ���գ����ù���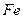 ��
��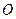 �����ʵ���֮��n(
�����ʵ���֮��n(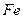 )��n(
)��n(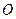 )="6:"
)="6:"  ��
�� mol��
mol�� ��
�� �Ĺ�ϵ���ߡ�
�Ĺ�ϵ���ߡ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��5 g | B��10 g |
| C��15 g | D��10.5 g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��H2S | B��Cl2 |
| C��HCl | D��CO2? |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���٢� | B���ڢܢ� | C���ڢܡ��� | D���ۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��12 | B��15 | C��28 | D��32 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��ʯ��ˮ | B���������� | C������ | D���Ȼ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��Ũ���������ˮ�ԣ������ʹ����̿�� |
B���ڷ�ӦHCOOH CO����H2O�У�ŨH2SO4ֻ������ˮ�� CO����H2O�У�ŨH2SO4ֻ������ˮ�� |
C���ڷ�ӦCu+2H2SO4(Ũ) CuSO4+SO2��+2H2O�У�ŨH2SO4ֻ���������� CuSO4+SO2��+2H2O�У�ŨH2SO4ֻ���������� |
| D��Ũ���������ˮ�ԣ������ʹCuSO4��5H2Oת��ΪCuSO4 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com