
| A. | 氯原子 | B. | 硫离子 | C. | 溴离子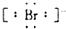 | D. | 钙离子Ca2+ |
分析 A.氯原子最外层有7个电子,据此判断即可;
B.硫离子为硫原子得到2个电子形成的阴离子,需要加中括号,据此解答即可;
C.溴离子为溴原子得到一个电子形成的阴离子;
D.钙离子为钙原子失去最外层2个电子形成的阳离子,阳离子与离子符号相同,据此解答即可.
解答 解:A.氯原子最外层电子数为7,电子式为 ,故A正确;
,故A正确;
B.硫离子为阴离子,电子式中需要标出所带电荷及最外层电子,硫离子的电子式为: ,故B错误;
,故B错误;
C.溴离子为阴离子,电子式中需要标出所带电荷及最外层电子,溴离子的电子式为: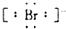 ,故C正确;
,故C正确;
D.钙离子的电子式用离子符号表示,为Ca2+,故D正确,
故选B.
点评 本题主要考查化学用语-电子式的书写,把握化学用语的规范使用,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | CH4>H2>HCl | B. | CH4>N2>HCl | C. | H2>HCl>CH4 | D. | HCl>CH4>H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用锌片替换铁片与稀硫酸反应 | B. | 将铁片与稀硫酸反应的温度升高 | ||
| C. | 用铁粉替换铁片与稀硫酸反应 | D. | 用浓硝酸替换稀硫酸与铁片反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 氯水应保存在棕色瓶中,久置的氯水,pH值减小 | |
| B. | 新制饱和氯水中存在4个平衡 | |
| C. | 在一定浓度的氯水中加小苏打,$\frac{c(HClO)}{c(C{l}^{-})}$变小 | |
| D. | 饱和氯水与石灰石的反应是制取较浓HClO溶液的重要方法 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 推广燃煤脱硫技术,可以防治SO2、CO的污染 | |
| B. | 绿色化学的核心是应用化学原理对环境污染进行治理 | |
| C. | 无论是风力发电还是潮汐发电,都是将化学能转化为电能 | |
| D. | 垃圾是放错地方的资源,应分类回收利用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液中c(OH-)=$\frac{1000b+c(H+)V}{V}$ mol/L | |
| B. | 溶质的物质的量浓度c=$\frac{1000a}{17V}$ mol/L | |
| C. | 溶质的质量分数w=$\frac{a}{ρV-a}$×100% | |
| D. | 向上述溶液中再加入VmL水后,所得溶液中溶质的质量分数小于0.5w |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由甲烷制四氯化碳,由乙烯与水反应制乙醇 | |
| B. | 由苯硝化制硝基苯,由乙醇遇到热的CuO固体得到单质铜 | |
| C. | 由苯和液溴制溴苯,由乙烯与溴水反应制1,2-二溴乙烷 | |
| D. | 由乙酸和乙醇制乙酸乙酯,由乙酸乙酯水解制乙酸和乙醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com