
| A. | 氨气是一种有强烈刺激气味的气体 | |
| B. | 氨气能被氧化为NO,是工业生产硝酸的重要原料之一 | |
| C. | 铵盐易和碱反应生成具有挥发性的氨气,在实验室中用NH4Cl和Ca(OH)2的混合物制取氨气 | |
| D. | 氨气极易溶于水,可用作制冷剂 |
分析 A、依据氨气的物理性质判断,氨气是一种强烈刺激性气味的气体;
B、氨气的催化氧化生成一氧化氮气体;
C、固体铵盐和氢氧化钙加热反应生成氨气;
D、氨气做制冷剂的依据是利用液氨挥发带走能量.
解答 解:A、氨气的物理性质可知,氨气是一种具有强烈刺激性气味的气体,故A正确;
B、氨气的催化氧化生成一氧化氮气体,一氧化氮和氧气反应生成二氧化氮,二氧化氮和水反应生成硝酸和一氧化氮,故B正确;
C、固体铵盐和氢氧化钙加热反应生成氨气,在实验室中用NH4Cl和Ca(OH)2的混合物制取氨气,故C正确;
D、氨气做制冷剂的依据是利用氨气易液化,液氨挥发带走能量,故D错误;
故选D.
点评 本题考查了氨气的性质,物质的制备和性质应用,掌握基础是关键,题目较简单.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | ②③ | C. | ③④ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
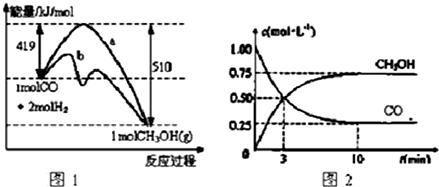
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(A)=0.5mol•L-1•s-1 | B. | v(B)=0.3mol•L-1•s-1 | ||
| C. | v(C)=0.8mol•L-1•s-1 | D. | v( D )=1.0mol•L-1•s-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2、O3 | B. | H2SO4、H2CO3 | C. | SO2、NO | D. | Na2SO3、KClO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com