
【题目】PbO2、KMnO4、Cl2、FeCl3、CuCl2的氧化性依次减弱。下列反应不可能发生的是( )
A.Cu+2Fe3+=Cu2++2Fe2+
B.5Pb2++2![]() +2H2O=5PbO2↓+2Mn2++4H+
+2H2O=5PbO2↓+2Mn2++4H+
C.Cu+Cl2 ![]() CuCl2
CuCl2
D.10Cl-+2![]() +16H+=2Mn2++5Cl2↑+8H2O
+16H+=2Mn2++5Cl2↑+8H2O
【答案】B
【解析】
由题意知:PbO2、KMnO4、Cl2、FeCl3、CuCl2的氧化性依次减弱,依据氧化还原反应中氧化剂的氧化性强于氧化产物的氧化性判断解答。
A、Cu+2Fe3+=Cu2++2Fe2+,反应中三价铁为氧化剂,铜离子为氧化产物,三价铁氧化性大于铜离子氧化性,与题意符合,故A不符合题意;
B、5Pb2++2![]() +2H2O=5PbO2↓+2Mn2++4H+,反应中高锰酸根离子为氧化剂,二氧化铅为氧化产物,高锰酸根离子氧化性强于二氧化铅,与题意不相符,故B符合题意;
+2H2O=5PbO2↓+2Mn2++4H+,反应中高锰酸根离子为氧化剂,二氧化铅为氧化产物,高锰酸根离子氧化性强于二氧化铅,与题意不相符,故B符合题意;
C、Cu+Cl2 ![]() CuCl2,反应中氯气为氧化剂,氯化铜为氧化产物,氯气氧化性大于铜离子,与题意符合,故C不符合题意;
CuCl2,反应中氯气为氧化剂,氯化铜为氧化产物,氯气氧化性大于铜离子,与题意符合,故C不符合题意;
D、10Cl-+2![]() +16H+=2Mn2++5Cl2↑+8H2O,反应中高锰酸根离子为氧化剂,氯气为氧化产物,高锰酸根离子氧化性强于氯气,符合题意,故D不符合题意;
+16H+=2Mn2++5Cl2↑+8H2O,反应中高锰酸根离子为氧化剂,氯气为氧化产物,高锰酸根离子氧化性强于氯气,符合题意,故D不符合题意;
故选B。


科目:高中化学 来源: 题型:
【题目】萜类化合物广泛存在于动植物体内,关于下列萜类化合物的说法正确的是( )
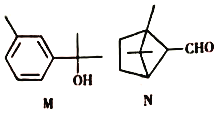
A. M和N互为同分异构体
B. M分子中所有碳原子均处于同一平面上
C. N与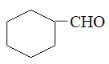 属于同系物
属于同系物
D. M和N均能使酸性KMnO4溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组类比镁在二氧化碳中的燃烧反应,认为钠和二氧化碳也可以发生反应,他们对钠在CO2气体中燃烧进行了下列实验:
(1)若用下图装置制备CO2,则发生装置中反应的离子方程式为_________。
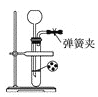
(2)将制得的CO2净化、干燥后由a口缓缓通入下图装置,待装置中的空气排净后点燃酒精灯,观察到玻璃直管中的钠燃烧,火焰为黄色。待冷却后,管壁附有黑色颗粒和白色物质。
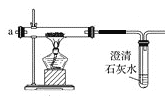
①能说明装置中空气已经排净的现象是_________。
②若未排尽空气就开始加热,则可能发生的化学反应方程式主要为_________。
(3)若钠着火,可以选用的灭火物质是_________。
A.水 B.泡沫灭火剂 C.干沙土 D.二氧化碳
(4)该小组同学对管壁的白色物质的成分进行讨论并提出假设:
Ⅰ.白色物质可能是Na2O; Ⅱ.白色物质可能是Na2CO3; Ⅲ.白色物质还可能是_________。
(5)为确定该白色物质的成分,该小组进行了如下实验:
实验步骤 | 实验现象 |
①取少量白色物质于试管中,加入适量水,振荡,样品全部溶于水,向其中加过量的CaCl2溶液 | 出现白色沉淀 |
②静置片刻,取上层清液于试管中,滴加无色酚酞试液 | 无明显现象 |
①通过对上述实验的分析,你认为上述三个假设中,___成立(填序号)。
②由实验得出:钠在CO2中燃烧的化学方程式为_____;每生成1mol氧化产物,转移的电子数为____。
(6)在实验(2)中还可能产生另一种尾气,该气体为________;处理该尾气的方法为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硝基苯是制造染料的重要原料,某同学在实验室里用如图所示装置制取硝基苯,主要步骤如下:

①在大试管里将2 mL浓硫酸和1.5 mL浓硝酸混合,摇匀,冷却到50~60 ℃以下;然后逐滴加入1 mL苯,边滴边振荡试管。
②按图连接好装置,将大试管放入60 ℃的水浴中加热10分钟。
完成下列填空:
(1)指出上图中的错误:__________、____________。
(2)向混合酸中加入苯时,“逐滴加入”“边滴边振荡试管”的目的是__________________________。
(3)反应一段时间后,混合液明显分为两层,上层主要物质是________(填物质名称)。把反应后的混合液倒入盛有冷水的烧杯里,搅拌,可以看到________(填字母)。
a.水面上是含有杂质的硝基苯
b.水底有苦杏仁味的液体
c.烧杯中的液态有机物只有硝基苯
d.有无色、油状液体浮在水面
(4)为了获得纯硝基苯,实验步骤:①水洗、分液;②将粗硝基苯转移到盛有__________的烧杯中洗涤、用__________(填仪器名称)进行分离;③__________;④干燥;⑤__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某树脂的结构片断如图所示,下列关于该树脂的说法不正确的是( )(图中~~~表示链延长)
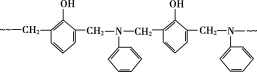
A.合成该树脂的反应为缩聚反应
B.理论上合成该树脂的原料比例相同
C.合成该树脂的单体之一甲醛可由甲醇氧化得到
D.该树脂难溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用惰性电极电解物质的量浓度相同、体积比为1∶2的CuSO4和NaCl的混合溶液,可能发生的反应有( )
①2Cu2++2H2O![]() 2Cu+4H++O2↑
2Cu+4H++O2↑
②Cu2++2Cl-![]() Cu+Cl2↑
Cu+Cl2↑
③2Cl-+2H+![]() H2↑+Cl2↑
H2↑+Cl2↑
④2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
A.①②③ B.①②④ C.②③④ D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,A是可用来对自来水进行消毒的黄绿色单质气体,A、B、C、D、E都含X元素,其转化关系如图所示:
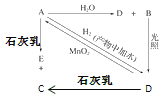
(1)请分别写出下列物质的化学式(如为溶液请填溶质的化学式):
A________、B________、D________。
(2)写出下列反应的化学方程式或离子方程式(请注明反应条件):
A+H2O(离子方程式):_____________;
A+石灰乳(化学方程式):______________;
E露置在空气中的第1个化学方程式:___________。
(3)漂白粉的有效成分是________(化学名称),保存漂白粉的方法__________、______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图中,甲是电解饱和食盐水,乙是铜的电解精炼,丙是电镀,回答:

(1)b极上的电极反应式为__,甲电池的总反应化学方程式是__。
(2)在粗铜的电解过程中,图中c电极的材料是__(填“粗铜板”或“纯铜板”);在d电极上发生的电极反应为__;若粗铜中还含有Au、Ag、Fe等杂质,则沉积在电解槽底部(阳极泥)的杂质是__,电解一段时间后,电解液中的金属离子有__。
(3)如果要在铁制品上镀镍(二价金属,相对原子质量59),则f电极的材料是__(填“铁制品”或“镍块”,下同),e电极的材料是__。
(4)若e电极的质量变化118 g,则a电极上产生的气体在标准状况下的体积为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
(1)25 ℃下,0.1mol/L氨水的电离度为1%,则此温下,该溶液的pH=______。
(2)25 ℃下,pH=2的硫酸溶液Va mL与pH=10的NaOH溶液Vb mL恰好中和,则,Va:Vb=___________。
(3)某温下,水的离子积常数KW=1.0×10-13。该温下,0.2mol·L-1的NaHSO4溶液与0.2mol·L-1的Ba(OH)2溶液等体积混合,混合后溶液的pH=______。
(4)一定条件下,可逆反应A2(g)+B2(g)2AB(g)达到化学平衡,经测定平衡时c(A2)=0.5 mol·L-1,c(B2)=0.1 mol.L-1,c(AB)=1.4 mol·L-1,若A2、B2、AB的起始浓度分别以a、b、c表示。请回答:
①a、b应满足的关系是_________。
②a的取值范围是___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com