
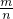 计算其摩尔质量,摩尔质量在数值上等于其相对分子质量,从而确定该金属的原子量.
计算其摩尔质量,摩尔质量在数值上等于其相对分子质量,从而确定该金属的原子量.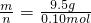 =95g?mol-1;摩尔质量在数值上等于其相对分子质量,所以其相对分子质量为95,其相对分子质量=其相对原子质量+35.5×2=95,所以该金属元素的相对原子质量为24.
=95g?mol-1;摩尔质量在数值上等于其相对分子质量,所以其相对分子质量为95,其相对分子质量=其相对原子质量+35.5×2=95,所以该金属元素的相对原子质量为24.

 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
(10分)进行下列化学基本量的计算,并将结果直接填入空格中。
⑴0.1摩H2SO4约含__________个H原子,溶于水后电离出__________mol SO42-。
⑵36克水与__________g CO2具有相同的氧原子数。
⑶71gNa2SO4中所含Na+的物质的量为__________mol。
(4)在9.5g某二价金属的氯化物中含0.2molCl—,此氯化物的摩尔质量为 ;该金属元素的相对原子质量为 。
(5)标准状况是指 ℃, Pa;在标准状况下,0.5molN2的体积都约为 L,质量为 g。
查看答案和解析>>
科目:高中化学 来源:2014届甘肃省兰州市高一上学期期中考试化学试卷 题型:填空题
(10分)进行下列化学基本量的计算,并将结果直接填入空格中。
⑴0.1摩H2SO4约含__________个H原子,溶于水后电离出__________mol SO42-。
⑵36克水与__________g CO2具有相同的氧原子数。
⑶71gNa2SO4中所含Na+的物质的量为__________mol。
(4)在9.5g某二价金属的氯化物中含0.2mol Cl—,此氯化物的摩尔质量为 ;该金属元素的相对原子质量为 。
(5)标准状况是指 ℃, Pa;在标准状况下,0.5molN2的体积都约为 L,质量为 g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com