
【题目】硝酸工业尾气中的氮氧化合物NOx(NO、NO2、N2O4)常用的处理方法有以下两种:
①碱液(Na2CO3或NaOH溶液)吸收法。用Na2CO3溶液吸收反应原理如下:
NO + NO2 + Na2CO3 == 2NaNO2 + CO2;2NO2 + Na2CO3 == NaNO2 + NaNO3 + CO2
②氨的催化氧化法,反应原理是:NOx + NH3![]() N2 + H2O
N2 + H2O
现将标准状况下2.016 L氮氧化合物NOx 通入50 mL 1.0 mol·L-1的Na2CO3溶液,恰好反应完全,且测得反应后溶液中n(NO2-)∶n(NO3-) = 4∶1,下列说法正确的是
A. 混合气体中V(N2O4) = 0.336 L
B. 混合气体中n(NO)∶n(NO2) = 1∶5
C. NOx能够完全被Na2CO3溶液吸收,则x ≤ 1.5
D. 如采用氨的催化氧化法处理,理论消耗n(NH3) = ![]() mol
mol
【答案】D
【解析】
(1)用Na2CO3溶液吸收:由方程式NO + NO2 + Na2CO3 == 2NaNO2 + CO2和2NO2 + Na2CO3 == NaNO2 + NaNO3 + CO2可知,NO单独不能被吸收,NO和NO2混合气体被Na2CO3溶液完全吸收,满足n(NO2):n(NO)≥1,当n(NO2):n(NO)=1时x值最小,x最小值为![]() =1.5,即x
=1.5,即x![]() 1.5;
1.5;
(2)2.016 L氮氧化合物的物质的量为![]() ,其中含有NO、NO2、N2O4三种气体,由方程式NO + NO2 + Na2CO3 == 2NaNO2 + CO2和2NO2 + Na2CO3 == NaNO2 + NaNO3 + CO2,把N2O4折换成NO2,恰好反应,溶液溶质为NaNO2、NaNO3,
,其中含有NO、NO2、N2O4三种气体,由方程式NO + NO2 + Na2CO3 == 2NaNO2 + CO2和2NO2 + Na2CO3 == NaNO2 + NaNO3 + CO2,把N2O4折换成NO2,恰好反应,溶液溶质为NaNO2、NaNO3,
由N元素守恒可知①n(NaNO2)+n(NaNO3)=n(NO2)+2n(N2O4)+n(NO),
由Na元素可知②2n(Na2CO3)=n(NaNO2)+n(NaNO3),
已知n(NO2)+n(N2O4)+n(NO)=0.09mol,
而n(NO2)+2n(N2O4)+n(NO)= n(NaNO2)+n(NaNO3)=2n(Na2CO3)=2×0.05L×1.0mol/L=0.1mol,
解得,n(N2O4)=0.01mol,V(N2O4)=0.01mol×22.4L/mol=0.224L,
因n(NO2-)∶n(NO3-) = 4∶1,n(NaNO2)+n(NaNO3)=0.1mol,
解得,n(NaNO2)=0.08mol,n(NaNO3)=0.02mol,
由方程式可知,2NO2 + Na2CO3 == NaNO2 + NaNO3 + CO2,
0.04mol 0.02mol 0.02mol
NO + NO2 + Na2CO3 == 2NaNO2 + CO2,
0.03mol 0.03mol (0.08mol-0.02mol)
所以0.09mol氮氧化物中含有0.03molNO、0.01molN2O4和(0.07mol-0.01mol×2)=0.05molNO2,
n(NO)∶n(NO2)= 0.03mol:0.05mol=3:5,
(3)氨的催化氧化法:因为在氨催化还原法反应中,NO、NO2、N2O4中的N分别由+2价和+4价→0价,NH3中的N由-3价→0.根据得失电子相等的原理有:
0.03mol![]() 2+0.01mol
2+0.01mol![]() 2
2![]() 4+0.05mol
4+0.05mol![]() 4=n(NH3)
4=n(NH3)![]() 3,
3,
解得n(NH3)=![]() mol,即如采用氨的催化氧化法处理,理论消耗n(NH3) =
mol,即如采用氨的催化氧化法处理,理论消耗n(NH3) = ![]() mol。
mol。
A. 根据以上分析,混合气体中V(N2O4) = 0.224 L,故A错误;
B. 根据以上分析,混合气体中n(NO)∶n(NO2) = 0.03mol:0.05mol=3:5,故B错误;
C. 根据以上分析,NOx能够完全被Na2CO3溶液吸收,则x![]() 1.5,故C错误;
1.5,故C错误;
D. 如采用氨的催化氧化法处理,理论消耗n(NH3) = ![]() mol,故D正确。
mol,故D正确。
答案选D。


 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案科目:高中化学 来源: 题型:
【题目】在两份相同的Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如右图所示。下列分析不正确的是( )

A. ①代表滴加H2SO4溶液的变化曲线
B. b点,溶液中大量存在的离子是Na+、OH–
C. c点,两溶液中含有相同量的OH–
D. a、d两点对应的溶液均显中性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(一)镓、硒、硅等元素的化合物是生产第三代太阳能电池的重要材料。已知:SeO2在常温下是白色的晶体,熔点为340-350℃,则SeO2晶体属于____晶体,SeO2中Se原子采取的杂化类型为___。
(二)A、X、Y、Z、W、M、G等原子序数一次增大的前四周期元素
元素 | 相关信息 |
A | 原子核外电子总数与其周期数相同 |
X | 其羞态原子的L层中有3个未成对电子 |
Y | 荃态原子的2p轨道上有一个电子的自旋方向与2p轨道上其它电子的自旋方向相反 |
Z | 原子核外p电子数比s电子数多l个 |
W | 原子的第一至第四电离能(kJ·mol-1)分别是:I1=578,I2=1817 I3=2745 I4=11575 |
M | 元素的主族数与周期数相差4 |
G | 其基态原子最外层电子数为1,其余各电子层均充满电子 |
(1)画出W基态原子的核外电子排布图______。
(2)A2Y的VSEPR模型名称为____。
(3)已知为X2Y分子中Y原子只与一个X原子相连,请根据等电子原理,写出X2Y的电子式____。
(4)X、G形成的某种化合物的晶胞结构如图所示,则其化学式为______。

(5)已知Z和M形成的化合物的晶体密度为pg·cm-3,阿伏加德罗常效为NA,该晶体中两个距离最近的Z离子中心间距离为_____cm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生活污水中的氮和磷主要以铵盐和磷酸盐的形式存在,可用电解法从溶液中除去。有Cl-存在时。除氮原理如图1所示。主要依靠有效氯(HClO、ClO-)将NH4+或NH3氧化为N2。在不同pH条件下进行电解时,氮的去除率和水中有效氯浓度与溶液pH的关系如图2所示。
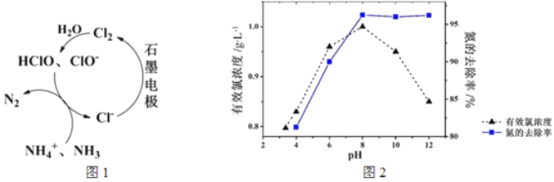
下列说法不正确的是
A. pH=3时,主要发生ClO-氧化NH3的反应
B. pH>8时,有效氯浓度随pH的增大而减小
C. pH>8时,NH4+转变为NH3·H2O,且有利于NH3逸出
D. pH<8时,氮的去除率随pH的减少而下降的原因是c(HClO)减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知一定条件下硝酸铵受热分解的化学方程式为:5NH4NO3![]() 2HNO3+4N2↑+9H2O,下列说法正确的是( )
2HNO3+4N2↑+9H2O,下列说法正确的是( )
A. 分解反应都是氧化还原反应B. N2是还原产物,HNO3是氧化产物
C. 被氧化与被还原的氮原子数之比为3∶5D. 每生成4mol N2转移15mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环氧乙烷(![]() )、环氧丙烷(
)、环氧丙烷(![]() )都是重要的化工原料且用途广泛。回答下列问题:
)都是重要的化工原料且用途广泛。回答下列问题:
(1)已知:
①![]()
![]()
②2![]()
![]()
![]()
③![]()
![]()
![]()
![]() _____
_____![]()
(2)某温度下,物质的量均为1mol的CH2=CH2和O2在0.5L的刚性容器内发生反应③,5min后反应达到平衡,气体总压减少了20%。
①平衡时CH2=CH2(g)的转化率为____,达到平衡后,欲增加CH2=CH2(g)的平衡转化率,可采取的措施是____(填一条措施即可)。
②0~5min内,环氧乙烷的生成速率为____。
③该反应的平衡常数K_____(精确到0.01)。
④当进料气CH2=CH2和O2的物质的量不变时,T1℃时达到反应平衡,请在图1中画出温度由T1℃变化到T2℃的过程中乙烯的转化率与温度的关系____。
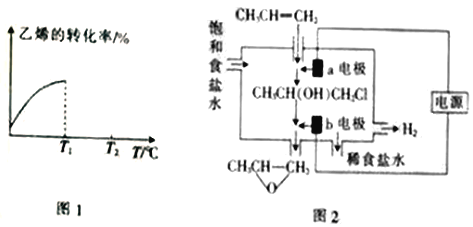
(3)将丙烯与饱和食盐水的电解产物反应,转化为氯丙醇[CH3CH(OH)CH2Cl][已知:CH3CH=CH2+H2O+Cl2→CH3CH(OH)CH2Cl+HCl],氯丙醇进一步反应生成环氧丙烷,其电解简易装置如图2所示。
①a电极上的电极反应式为______。
②b电极区域生成环氧丙烷的化学方程式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质或物质间反应可能包括多步反应,其总的离子方程式正确的是
A. 向NaClO溶液中通入过量SO2:ClO-+SO2+H2O===HClO+HSO3-
B. Na2S投入水中:S2-+2H2O![]() H2S+2OH-
H2S+2OH-
C. 向含1 mol AlCl3溶液中投入4 mol Na:Al3++4Na+2H2O===AlO2-+4Na++2H2↑
D. 向明矾溶液中滴加Ba(OH)2溶液,恰好使SO42-沉淀完全:2Al3++3SO42-+3Ba2++6OH-===Al(OH)3↓+3BaSO4↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某新型电池,以NaBH4(B的化合价为+3价)和H2O2作原料,该电池可用作深水勘探等无空气环境电源,其工作原理如图所示。下列说法正确的是
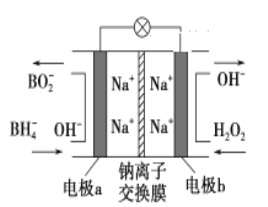
A. 电池工作时Na+从b极区移向a极区
B. a极上的电极反应式为:BH4-+8OH--8e-===BO2-+6H2O
C. 每消耗3 mol H2O2,转移3 mol e-
D. b极上的电极反应式为:H2O2+2e-+2H+===2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工厂排放的SO2烟气对环境造成污染,某企业用下图流程综合处理,下列有关说法正确的是

A. 二氧化硫吸收塔中发生的反应为SO2+SO32—+H2O=2HSO3—
B. 氨气吸收塔中发生的反应为HSO3—+OH-=H2O+SO32—
C. 上述流程利用的是氧化还原反应原理
D. 上述流程可循环利用的物质有2种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com