
| A. | NaCl溶液(BaCl2):加Na2SO4溶液,过滤 | |
| B. | NaCl溶液(I2):加酒精,萃取 | |
| C. | KNO3溶液(AgNO3):加NaCl溶液,过滤 | |
| D. | KNO3溶液(I2):加CCl4,萃取 |
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 盐酸、空气、醋酸、干冰 | B. | 铁、海水、硫酸钠、乙醇 | ||
| C. | 硫酸、蔗糖、烧碱、石灰石 | D. | 胆矾、漂白粉、氯化钾、硫酸钡 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe Cu Al Ag Mg | B. | Al Cu Mg Ag Fe | ||
| C. | Mg Cu Al Ag Fe | D. | Mg Ag Al Cu Fe |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
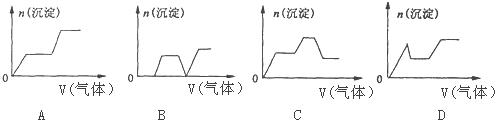
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 该硫酸的物质的量浓度为9.2 mol•L-1 | |
| B. | 1 mol 铁加入到足量的该硫酸中,可产生2 g H2 | |
| C. | 该硫酸与等质量的水混合所得溶液的物质的量浓度大于9.2 mol•L-1 | |
| D. | 配制200 mL 4.6 mol•L-1的硫酸溶液需取该硫酸50 mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原溶液一定显中性 | |
| B. | 原溶液中肯定不存在的离子有Fe2+、Ba2+ | |
| C. | 无法确定原溶液中是否存在Cl-、Na+、SO42- | |
| D. | 原溶液中肯定存在的离子有Fe2+、SO42-、I- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl-Cl键比H-H键的键能小,是因为Cl原子比H原子的非金属性强 | |
| B. | H2(g)与Cl2(g)反应生成2 molHCl(g),反应的△H=183 kJ/mol | |
| C. | H2(g)与Cl2(g)反应生成2 molHCl(g),反应的△H=-183 kJ/mol | |
| D. | H2(g)与Cl2(g)反应生成1 molHCl(g),反应的△H=-183 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若向该溶液中加入过量的稀硫酸,溶液中阴离子种类仍不变 | |
| B. | 若向该溶液中加入足量的NaOH溶液,充分反应后,过滤、洗涤、灼烧,最终所得固体的质量为72g | |
| C. | 若向该溶液中加入过量的稀硫酸和KSCN溶液,溶液显血红色 | |
| D. | 该溶液中一定不含Al3+、Ba2+、Cl- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com