
| A. | 苯和甲苯都能与浓硝酸发生苯环上的取代反应 | |
| B. | 苯和甲苯都能使酸性高锰酸钾溶液褪色 | |
| C. | 苯和己炔都能使溴的四氯化碳溶液发生化学反应而褪色 | |
| D. | 苯和乙烷与卤素单质发生取代反应都需要铁作催化剂 |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
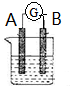 如图所示为原电池装置示意图.
如图所示为原电池装置示意图.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | +244.1 kJ•mol-1 | B. | -488.3 kJ•mol-1 | C. | -996.6 kJ•mol-1 | D. | +996.6 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ①②④ | C. | ②③ | D. | ④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
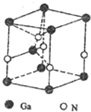 碳、氮元素及其化合物在生产、生活和科学研究等方面有着重要的作用研究它们的结构与性质意义重大.请回答下列有关问题:
碳、氮元素及其化合物在生产、生活和科学研究等方面有着重要的作用研究它们的结构与性质意义重大.请回答下列有关问题: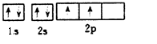 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C6H12O6(s)+6O2(g)=6CO2(g)+6H2O(l)△H1 | B. | S(s)+3/2O2(g)=SO3(s)△H2 | ||
| C. | CH4(g)+2O2(g)=2H2O(l)+CO(g)△H3 | D. | 2CO(g)+O2(g)=CO2(g)△H4 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com