
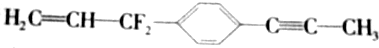
 为已知结构,下列叙述中正确的是( )
为已知结构,下列叙述中正确的是( )| A. | 除苯环外的其余碳原子有可能都在同一条直线上 | |
| B. | 在同一平面上的原子最多有19个 | |
| C. | 12个碳原子不可能都在同一个平面上 | |
| D. | 12个碳原子有可能都在同一个平面上 |
分析 根据常见的有机化合物中甲烷是正四面体结构,乙烯和苯是平面型结构,乙炔是直线型结构,其它有机物可在此基础上进行共线、共面分析判断,注意单键可以旋转.
解答 解:A.双键相连的碳与CF2的碳不在同一直线上,故A错误;
B. 为分子中,CF2中C原子处于苯中H原子的位置,苯环平面与碳碳双键形成的平面通过旋转碳碳单键可以处于同一平面,乙炔是直线型结构,所以最多有12个C原子共面.在甲基上可能还有1个氢原子共平面,苯环上4个氢原子共平面,双键上3个氢原子共平面,总计得到可能共平面的原子有20个,故B错误;
为分子中,CF2中C原子处于苯中H原子的位置,苯环平面与碳碳双键形成的平面通过旋转碳碳单键可以处于同一平面,乙炔是直线型结构,所以最多有12个C原子共面.在甲基上可能还有1个氢原子共平面,苯环上4个氢原子共平面,双键上3个氢原子共平面,总计得到可能共平面的原子有20个,故B错误;
C. 为分子中,CF2中C原子处于苯中H原子的位置,苯环平面与碳碳双键形成的平面通过旋转碳碳单键可以处于同一平面,乙炔是直线型结构,所以最多有12个C原子共面,故C错误D正确.
为分子中,CF2中C原子处于苯中H原子的位置,苯环平面与碳碳双键形成的平面通过旋转碳碳单键可以处于同一平面,乙炔是直线型结构,所以最多有12个C原子共面,故C错误D正确.
故选D.
点评 本题考查有机物结构中共面、共线问题,难度中等,关键是空间想象,做题时注意从甲烷、乙烯、苯和乙炔的结构特点判断有机分子的空间结构,单键可以旋转.


科目:高中化学 来源: 题型:选择题
| A. | 71 g Cl2含有的氯原子数目为NA | |
| B. | 标准状况下,2.24 L水所含的分子数为0.1 NA | |
| C. | 1 mol•L-1A1Cl3溶液中含有的Cl-数目为3 NA | |
| D. | 2.4 g金属镁变成镁离子时失去的电子数目为0.2 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
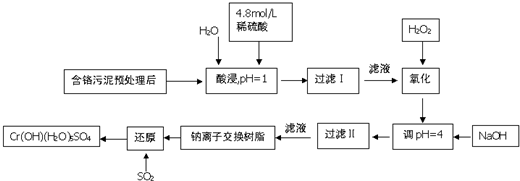
| 阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Cr3+ |
| 开始沉淀时的pH | 2.7 | 7.0 | 9.3 | 3.7 | - |
| 沉淀完全是的pH | 3.7 | 9.0 | 11.1 | 8 | 9(>9溶解) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加热法可以除去氯化铵中的少量碘单质 | |
| B. | 向试液中滴加双氧水和KSCN溶液,溶液变为红色,则试液中一定含Fe2+ | |
| C. | 向某固体中滴加稀硫酸,产生气体能使澄清石灰石变浑浊,则该固体一定是苏打或小苏打 | |
| D. | 向含少量硫酸铁的硫酸铜溶液中加入过量的氧化铜,过滤,得到纯净硫酸铜溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
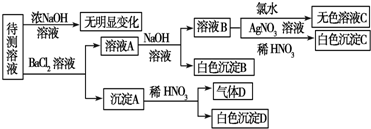
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
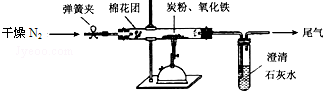
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com