
【题目】在一定温度下,固定体积为2L密闭容器中,发生反应:
2SO2(g)+O2(g)![]() 2SO3(g ) ΔH <0,n(SO2)随时间的变化如表:
2SO3(g ) ΔH <0,n(SO2)随时间的变化如表:
时间/min | 0 | 1 | 2 | 3 | 4 | 5 |
n(SO2)/mol | 0.20 | 0.16 | 0.13 | 0.11 | 0.08 | 0.08 |
则下列说法正确的是
A. 当v(SO2)=v(SO3)时,说明该反应已达到平衡状态
B. 用O2表示0~4 min内该反应的平均速率为0.005 mol/(L·min)
C. 平衡时再通入O2,平衡右移,O2转化率减小,SO2转化率增大
D. 若升高温度,则SO2的反应速率会变大,平衡常数K值会增大
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W有如图所示的转化关系:
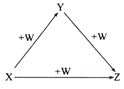
(1)若X单质的一种同素异形体是一种黑色的非金属单质,则Y转化为Z的化学方程式_____。
(2)若X为一种金属的氯化物,Y是一种常见的两性氢氧化物,W为化工常用的强碱,写出Y与W反应的离子方程式_____________。
(3)若X是一种活泼的金属单质,Z是一种淡黄色的化合物,则Z转化为W的化学方程式_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究NO2、SO2 、CO等大气污染气体的处理具有重要意义。
(1)NO2可用水吸收,相应的化学反应方程式为______________________。利用反应6NO2+8NH3 ![]() 7N2+12 H2O也可处理NO2。当转移1.2 mol电子时,消耗的NO2在标准状况下是__________L。
7N2+12 H2O也可处理NO2。当转移1.2 mol电子时,消耗的NO2在标准状况下是__________L。
2)已知:2SO2(g)+O2(g)![]() 2SO3(g) ΔH=-196.6 kJ·mol-1
2SO3(g) ΔH=-196.6 kJ·mol-1
2NO(g)+O2(g)![]() 2NO2(g) ΔH=-113.0 kJ·mol-1
2NO2(g) ΔH=-113.0 kJ·mol-1
则反应NO2(g)+SO2(g)![]() SO3(g)+NO(g)的ΔH=_________kJ·mol、1。
SO3(g)+NO(g)的ΔH=_________kJ·mol、1。
一定条件下,将NO2与SO2以体积比1︰2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是
a.体系压强保持不变
b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变
d.每消耗1 mol SO3的同时生成1 mol NO2
测得上述反应平衡时NO2与SO2体积比为1︰6,则平衡常数K=__________________。
(3)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)![]() CH3OH(g)。
CH3OH(g)。
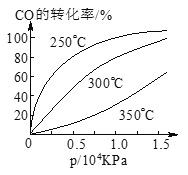
CO在不同温度下的平衡转化率与压强的关系如图所示。该反应ΔH___________0(填“>”或“ <”)。实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有BaCl2和NaCl混合溶液aL,将它均分成两份。一份滴加硫酸,使Ba2+完全沉淀;另一份滴加AgNO3溶液,使Cl-完全沉淀.反应中消耗xmolH2SO4、ymolAgNO3.据此得知原混合溶液中的c(Na+)为
A. (2y-4x) /amol·L-1 B. (y-2x) /amol·L-1
C. (2y-2x) /amol·L-1 D. (y-x) /amol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】固体氧化物燃料电池是以固体氧化锆—氧化钇为电解质,这种固体电解质在高温下允许氧离子(O2-)在其间通过。该电池的工作原理如下图所示,其中多孔电极a、b均不参与电极反应。
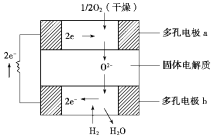
下列判断正确的是( )
A.有O2参加反应的a极为电池的负极
B.正极极的电极反应式为H2-2e-+O2-===H2O
C.a极对应的电极反应式为O2+2H2O+4e-===4OH-
D.该电池的总反应式为2H2+O2![]() 2H2O
2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据磷元素的原子结构示意图 ,做出如下推理,其中与事实不符的是
,做出如下推理,其中与事实不符的是
A. 磷元素位于元素周期表的第三周期、第ⅤA族
B. 磷原子不如氮原子和硫原子的得电子能力强
C. 磷单质不如氮气和硫单质的化学性质活泼
D. 磷的氢化物(PH3)受热时不如氮的氢化物(NH3)和硫的氢化物(H2S)稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学—选修5有机化学基础】邻苯二甲酸二乙酯![]() 是一种重要的工业塑化剂,其合成路线很多,下图就是其中的一种合成方法:
是一种重要的工业塑化剂,其合成路线很多,下图就是其中的一种合成方法:

已知以下信息:
① 有机化合物A可用来催熟水果。
② 有机化合物C的核磁共振氢谱显示其有3种不同化学环境的氢原子。

(1)A的化学名称是 ,B的结构简式为 。
(2)反应Ⅱ的试剂是 ,该反应类型为 。
(3)C生成D的化学方程式为 。
(4)E生成F的化学方程式为 。
(5)在G的同分异构体中,既能与新制的Cu(OH)2悬浊液在加热条件下反应生成砖红色沉淀,又能与碳酸钠反应生成二氧化碳,还能使FeCl3溶液显色的有 种,所有这些同分异构体中,不同化学环境氢原子的种数 (填“相同”“不相同”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在半导体工业中,有一道工序叫烧氢。烧氢的工艺流程如图所示。
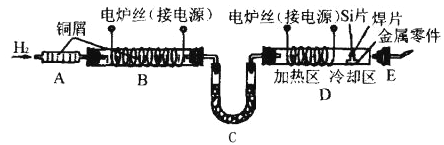
工作时,是将石英管D出口处氢气点燃。半导体硅片、焊片和金属零件从石英管口送入加热区,在氢气还原气氛中加热使焊片熔化,将单晶硅与金属零件焊接在一起。焊接后再将零件拉至冷却区,冷却后取出。烧氢工艺中的氢气纯度要求极高,工业氢气虽含氢量达99.9%,但仍含有极微量的水蒸气和氧气,所以点燃氢气前应检验氢气的纯度。试回答下列问题:
(1)装置B的作用是________;B中发生反应的化学方程式是________。
(2)装置C中的物质是________;C的作用是________。
(3)点燃氢气前将E(带导管胶塞)接在D出口处,目的是________。
(4)装置A是安全瓶,可以防止氢气燃烧回火,引起爆炸,其中填充大量纯铜屑的作用是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com