
下列说法中正确的是
A.1 L水中溶解了58.5 g NaCl,该溶液的物质的量浓度为1 mol/L
B.从1 L 2 mol/L的H2SO4溶液中取出0.5 L,该溶液的浓度为1 mol/L
C.配制500 mL 0.5 mol/L的CuSO4溶液,需62.5 g胆矾
D.中和100 mL 1 mol/L的H2SO4溶液,需NaOH 4 g
科目:高中化学 来源: 题型:
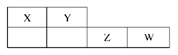
X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如下图所示。若Y原子的最外层电子数是次外层电子数的2倍,下列说法中正确的是( )
A.氢化物稳定性:X>Y
B.最高价氧化物对应的水化物的酸性:W>Y
C.4种元素的单质中,W单质的熔、沸点最高
D.干燥的W单质具有漂白性
查看答案和解析>>
科目:高中化学 来源: 题型:
高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,其与水的离子反应是:
4FeO42-+10H2O=4Fe(OH)3(胶体)+3O2↑+8OH-
工业上先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入一定量的KOH就可制得高铁酸钾。制备高铁酸钠的两种方法的主要反应原理如下:
湿法制备——2Fe(OH)3+3ClO-+4OH-=2FeO42-+3Cl-+5H2O;
干法制备——2FeSO4 +6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑。
下列有关说法中错误的是( )
A.高铁酸钾与水反应时,水发生氧化反应
B.干法中每生成1mol Na2FeO4共转移4mol电子
C.湿法中每生成1mol Na2FeO4共转移3mol电子
D.K2FeO4处理水时,不仅能杀菌,还能除去H2S、NH3等,并使悬浮杂质沉降
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下,有a.盐酸 b.硫酸 c.醋酸三种酸:
(1)当三种酸物质的量浓度相同时,c(H+)由大到小的顺序是 。
(2)同体积、同物质的量浓度的三种酸,中和NaOH的能力由大到小的顺序是 。
(3)若三者c(H+)相同时,物质的量浓度由大到小的顺序是 。
(4)当三者c(H+)相同且体积也相同时,分别放入足量的锌,相同状况下产生气体的体积由大到小的顺序是 。
(5)当三者c(H+)相同且体积相同时,同时加入形状、密度、质量完全相同的锌,若产生相同体积的H2(相同状况),则开始时反应速率的大小关系为 ,反应所需时间的长短关系是 。
(6)将c(H+)相同的三种酸均加水稀释至原来的100倍后,c(H+)由大到小的顺序是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于物质分类的说法正确的是
A.氯化铵、次氯酸都属于强电解质 B.漂白粉、石英都属于纯净物
C.金刚石、白磷都属于单质 D.葡萄糖、蛋白质都属于高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
浓H2SO4 密度1.84g/mL,物质的量浓度为18.4 mol/L , 质量分数为98% ,取10mL浓H2SO4和amL水混合得物质的量浓度为Cmol/L,质量分数为b%。下列组合正确的是
(1).若C=9.2则a>10 b>49% (2) 若C=9.2则a>10 b<49%
(3).若b=49则a=18.4 C<9.2 (4) 若b=49则a=18.4 C>9.2
A.(1) (3) B.(1) (4) C.(2) (3) D.(2) (4)
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)在标准状况下,a.6.72 L CH4气体 b.3.01×1023个HCl气体分子 c.13.6g H2S气体 d.0.2mol NH3,下列对这四种气体的关系从大到小的排列是(用上述序号表示)。
①四种气体的物质的量___________________________________;
②标准状况下四种气体的密度_____________________________;
③四种气体的质量_______________________________________。
(2)阿伏加德罗曾做过这样一个实验:一抽空的密闭容器重Mg,在标准状况下,盛满以相同物质的量混合的NO和H2的混合气体后,称量为(M+Q)g。把混合气体排尽,再充满SO2气体,为使天平平衡,应在托盘天平的________边托盘上放置________g砝码。
(3)将10g复盐CuSO4·x(NH4)2SO4·yH2O加到过量的NaOH溶液中加热,生成的氨气用100 mL 0.5mol/L硫酸全部吸收,多余的硫酸用2mol/L NaOH溶液中和,用去NaOH溶液25 mL。已知复盐中SO的质量分数为48%,则x=________,y=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
恒温恒容的三个密闭容器,N2(g)+3H2(g)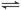 2NH3(g) △H=-92.4 kJ/mol。实验测得起始、平衡时的有关数据如下表。下列叙述正确的是
2NH3(g) △H=-92.4 kJ/mol。实验测得起始、平衡时的有关数据如下表。下列叙述正确的是
| 容器 编号 | 起始时各物质物质的量/mol | 平衡时反应中的能量变化 | ||
| N2 | H2 | NH3 | ||
| ① | 1 | 3 | 0 | 放出热量a kJ |
| ② | 2 | 3 | 0 | 放出热量b kJ |
| ③ | 2 | 6 | 0 | 放出热量c kJ |
A.放出热量a<b<92.4 B.三个容器内反应的平衡常数③>①>②
C.N2的转化率①<② D.达平衡时氨气的体积分数①>③
查看答案和解析>>
科目:高中化学 来源: 题型:
传统的自来水消毒常采用漂白粉等强氧化剂,但其产生的有机氯对人体有一定的危害。一种新型的消毒剂——高铁酸盐(如Na2FeO4或K2FeO4)能有效地杀灭水中的细菌和病毒,同时其产物在水中经过变化后能除去水中的微细悬浮物。在以上变化过程中不可能涉及的变化有( )
A . 电离 B. 水解 C. 置换反应 D. 氧化还原反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com