
硫化钠是由无水硫酸钠与炭粉在高温下反应制得。反应的化学方程式如下:
① Na2SO4+ 4C→ Na2S+ 4CO↑ ② Na2SO4+ 4CO→ Na2S+ 4CO2↑
(1)要制取Na2S 15.6 g,需原料芒硝(Na2SO4·10H2O)_____________mol。
(2)制得的Na2S固体中含少量Na2SO4、碳粉等杂质。称取该固体0.200 g,加适量水溶解后加入25.0 mL 0.100 mol/L的I2标准液,待反应完全后用0.100 mol/L Na2S2O3溶液滴定,消耗Na2S2O3溶液16.0 mL(已知:滴定时 Na2S2O3转化为Na2S4O6),则该Na2S的纯度为__________。
(3)① 若在反应过程中,产生CO和CO2混合气体的体积为44.8L(标准状况),生成Na2S的物质的量(n mol)的范围是__________< n < ___________;
② 若在上述过程中生成Na2S的质量为62.4 g,则混合气体中CO和CO2的体积比是多少?
(4)硫化钠晶体(Na2S·9H2O)放置在空气中,会缓慢氧化成Na2SO3·7H2O和Na2SO4·10H2O。现称取在空气中已部分氧化的硫化钠晶体25.76 g溶于水,加入足量用盐酸酸化的BaCl2溶液,过滤得沉淀5.62 g,放出H2S气体1.12 L(标准状况),求原硫化钠晶体的质量。
(1)0.2(2分)
(2)66.3%(2分)
(3)①0.5 1.0(2分) ② 2:3(3分)
(4)24g(5分,列式3分,计算过程及结果2分)
解析试题分析:(1)要制取Na2S 15.6 g,需原料芒硝。根据硫原子守恒可知,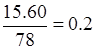 ,解得(Na2SO4·10H2O)0.2mol。
,解得(Na2SO4·10H2O)0.2mol。
(2)根据两步转化关系通过计算求得Na2S的纯度为 66.3%。
(3)①由反应①和②可得反应③:Na2SO4+ 2C Na2S + 2CO2↑根据反应①和反应③,由极值法得:消耗的碳单质的物质的量范围n的范围是:0.5 mol ~ 1 mol。②若在上述过程中生成Na2S的质量为62.4 g,即为0.8mol。设混合气体中CO和CO2的物质的量分别是x,a。则有
Na2S + 2CO2↑根据反应①和反应③,由极值法得:消耗的碳单质的物质的量范围n的范围是:0.5 mol ~ 1 mol。②若在上述过程中生成Na2S的质量为62.4 g,即为0.8mol。设混合气体中CO和CO2的物质的量分别是x,a。则有
①: Na2SO4+ 4C Na2S + 4CO
Na2S + 4CO
x mol x/4 mol x mol
根据反应③: Na2SO4+ 2C  Na2S + 2CO2
Na2S + 2CO2
a mol a/2 mol a mol
根据题意得: a mol + x mol ="2" mol
a/2mol + x/4 mol =" 0.8" mol,解得:a=1.2,x-0.8,则CO和CO2的体积比为3:2。
(4)5.62 g沉淀是硫酸钡和硫, 1.12 LH2S气体物质的量是0.05mol。设硫的物质的量为amol,硫酸钠的物质的量为bmol,则根据下列两个方程式可建立关系式:
2Na2S+ Na2SO3+6 HCl="6NaCl+" 3S↓+3H2O
2a/3 a/3 a
Na2S+ 2HCl= NaCl+H2S
0.05mol 0.05mol
233b+32a=5.62;再根据质量守恒:25.76 = a/3(126*2)+322b+(0.05+2a/3)*78,再根据硫原子守恒,求出原硫化钠晶体的质量24g。
考点:本题考查根据化学方程式进行计算。


科目:高中化学 来源: 题型:填空题
(1)相同物质的量的O2和O3,所含分子数目之比为_______,所含氧原子的物质的量之比为_________。
(2)在标准状况下,①4 g H2.②11.2 L O2.③1 mol H2O中,含原子数最多的是_ ___,体积最小的是_______。(填序号)
(3)标况下,将224L的HCl气体溶于835ml(ρ=1g/cm3)的水中,所得盐酸的密度为1.2g/cm3, 该盐酸的物质的量浓度___________.。
(4)某气体物质质量为6.4 g,含有6.02×1022个分子,则该气体的相对分子质量为_______。
(5)Na2CO3的摩尔质量是____________,0.5mol Na2CO3的质量是____________,含有________mol Na+,Na+的个数约为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(1)0.7 mol H2O的质量为____________,其中含有_________个水分子,氢原子的物质的量为__________。
(2)质量相同的H2、NH3、SO2、O3四种气体中,含有分子数目最少的是_________,在相同温度和相同压强条件下,体积最大的是___________。
(3)在_______mL 0.2 mo1·L-1 NaOH溶液(密度为1 g·cm-3)中含1g溶质;配制50mL0.2 mo1·L-1 CuSO4溶液,需要CuSO4·5H2O__________g。
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
配制250ml 1.0 mol/L 的Na2CO3溶液,需称取Na2CO3固体多少克?取配制好的溶液25ml,往其中逐滴滴加1.0 mol/L的H2SO4溶液15ml,求生成的气体在标准状况下的体积是多少升?
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
向100ml 1mol/L 的Al2(SO4)3 溶液中加入100ml NaOH溶液,得到7.8克白色沉淀,请问NaOH溶液物质的量浓度可能是多少?
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
铝及其化合物在生产生活中的应用广泛。
(1)Al4C3用于冶金及催化剂。与盐酸反应(产物之一是含氢量最高的烃)的化学方程式是: ;14.4g Al4C3与盐酸反应产生的气体是 L(标准状况)。
(2)AlN用于电子仪器。AlN中常混有少量碳,将一定量含杂质碳的AlN样品置于密闭反应器中,通入4.032L(标准状况下的)O2,在高温下充分反应后测得气体的密度为1.34g/L(已折算成标准状况,AlN不跟O2反应),则所得气体的摩尔质量为 g/mol,该气体的成分是 (写化学式),该样品中含杂质碳 g。
(3)氯离子插层镁铝水滑石是一种新型的离子交换材料。制备这种水滑石的过程是:MgCl2、AlCl3、NaOH、NaCl溶液,按一定比例混合,在65℃充分反应后,经过滤、洗涤、干燥得到该水滑石。为确定该水滑石的成分,进行如下操作:
①取26.65g样品,在高温下使其充分分解,得到金属氧化物和气体,气体依次通过足量的浓硫酸和浓氢氧化钠溶液,这两种液体分别增重9.9g和3.65g;将金属氧化物在无色火焰上灼烧,火焰仍无色。
②另取26.65g样品,加入足量的稀硝酸,使其完全溶解,再加入NaOH溶液至过量,最终得到11.6g白色沉淀。通过计算确定氯离子插层镁铝水滑石的化学式。
(4)氯离子插层镁铝水滑石在空气中放置,缓慢与CO2反应,部分氯离子会被碳酸根离子代替。26.65g样品在空气中放置一段时间后质量变为25.925g,则碳酸根离子代替部分氯离子的水滑石的化学式是 ,此过程的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
有铁和铝的混合物共5.5g,完全溶解于200mL 36.5%的浓盐酸(密度为1.2 g/mL)中,在标准状况下共收集到4.48L H2,求:
(1)浓盐酸的物质的量浓度为 。
(2)铁的质量为 ,铝的质量为 。
(3)将反应后剩余的溶液,用水稀释至500mL,求稀释后溶液中盐酸的物质的量浓度(HCl挥发忽略不计) 。
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
足量的锌加入100mL的盐酸溶液中反应,生成标准状况下的H24.48L。回答:
(1)盐酸溶液的物质的量浓度。
(2)取该盐酸溶液10mL,加水稀释至100mL,求稀释后所得溶液的物质的量浓度。
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
在200mL的混合溶液中,硝酸和硫酸的物质的量的浓度均为0.2mol/L,向该混合液中加入3.84g的铜,加热使其充分反应。试计算:
(1)理论上生成的一氧化氮(标准状况下)的体积是多少升?
(2)若反应后溶液的体积不发生变化,溶液中Cu2+物质的量浓度是多少?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com