
分析 ①苯和石蜡沸点不同;
②乙酸乙酯不溶于饱和碳酸钠溶液,乙酸与碳酸钠反应;
③丙烯含有碳碳双键,可与溴水发生加成反应;
④溴乙烷和苯的沸点不同.
解答 解:①苯和石蜡沸点不同,可用蒸馏的方法分离,故答案为:蒸馏;
②乙酸乙酯不溶于饱和碳酸钠溶液,乙酸与碳酸钠反应,则可加饱和碳酸钠溶液后,分液,以达到分离的目的,故答案为:加饱和碳酸钠溶液后,分液;
③丙烯含有碳碳双键,可与溴水发生加成反应,可通过溴水,洗气,故答案为:通过溴水,洗气;
④溴乙烷和苯的沸点不同,可用蒸馏的方法分离,故答案为:蒸馏.
点评 本题考查物质的分离、提纯,为高频考点,侧重考查学生的分析能力和实验能力,注意把握物质的性质的异同,把握实验的原理和方法,难度不大.


科目:高中化学 来源: 题型:多选题
| A. | 温度相同、体积相同的O2和O3 | B. | 质量相等、密度不等的C2H6和NO | ||
| C. | 质量相等、密度不等的CO和N2 | D. | 体积相等、密度相等的CO2和N2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子序数a>b>c>d | |
| B. | 最高价氧化物对应水化物的碱性B>A | |
| C. | 单质还原性A>B>C>D | |
| D. | 离子半径D(n+1)->Cn->An+>B(n+1)+ |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
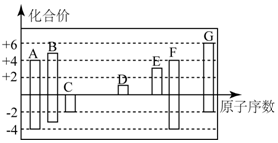 如图是部分短周期元素的常见化合价与原子序数的关系:
如图是部分短周期元素的常见化合价与原子序数的关系: ,其所含化学键类型为离子键和非极性键.
,其所含化学键类型为离子键和非极性键.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
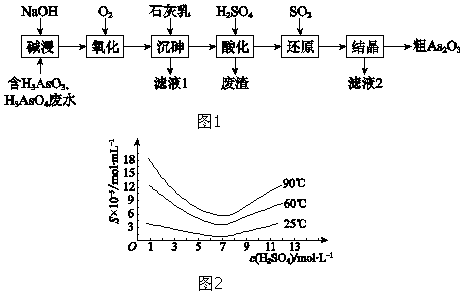
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲苯和水 | B. | 硝酸钾和氯化钠 | ||
| C. | 乙酸乙酯和甘油(丙三醇) | D. | 食盐水和泥沙 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 简单离子半径的大小顺序:rX>rY>rZ>rW | |
| B. | 元素Q和Z能形成QZ2型的共价化合物 | |
| C. | Z元素氢化物的沸点高于W元素氢化物的沸点 | |
| D. | X、Y、Z最高价氧化物的水化物之间两两不能发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com