
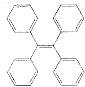
 有机物TPE具有聚集诱导发光特性,在光电材料领域应用前景广阔,其结构简式如图所示,下列说法正确的是( )
有机物TPE具有聚集诱导发光特性,在光电材料领域应用前景广阔,其结构简式如图所示,下列说法正确的是( )| A. | 该有机物的分子式为C26H22 | |
| B. | 该有机物属于苯的同系物 | |
| C. | 该有机物的一氯代物有4种 | |
| D. | 该有机物既可发生氧化反应,又可发生还原反应 |
分析 A.根据结构简式确定分子式;
B.苯的同系物中只含一个苯环且侧链为烷基;
C.该有机物中氢原子有3种,有几种氢原子,其一氯代物就有几种;
D.该物质为烃,能发生氧化反应,能与氢气发生加成反应.
解答 解:A.根据结构简式确定分子式为C26H20,故A错误;
B.苯的同系物中只含一个苯环且侧链为烷基,该物质中含有多个苯环且含有烯烃基,不是苯的同系物,故B错误;
C.该有机物中氢原子有3种,有几种氢原子,其一氯代物就有几种,所以有3种一氯代物,故C错误;
D.该物质为烃,且含有碳碳双键,能发生氧化反应,能与氢气发生加成反应,故D正确;
故选D.
点评 本题考查有机物结构和性质,为高频考点,明确官能团及其性质关系及物质结构是解本题关键,注意该分子中氢原子种类,题目难度不大.


 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源: 题型:选择题
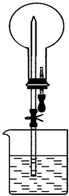 如图所示的装置中,干燥烧瓶中盛有某种气体,烧杯和滴管内盛放某种溶液.挤压滴管的胶头,下列与实验事实不相符的是( )
如图所示的装置中,干燥烧瓶中盛有某种气体,烧杯和滴管内盛放某种溶液.挤压滴管的胶头,下列与实验事实不相符的是( )| A. | SO2(饱和NaHSO3溶液) 无色喷泉 | B. | NH3(H2O含酚酞) 红色喷泉 | ||
| C. | H2S(CuSO4溶液) 黑色喷泉 | D. | HCl(AgNO3溶液) 白色喷泉 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 某溶液中滴加KSCN溶液呈无色,再滴加氯水后出现血红色,该溶液中含有Fe2+ | |
| B. | 某溶液中滴加NaOH溶液后再滴加CaCl2溶液出现白色沉淀,该溶液中含有CO32- | |
| C. | 某溶液中滴加氨水后再滴加NaOH溶液出现白色沉淀,该溶液中含有Al3+ | |
| D. | 某溶液中滴加足量稀盐酸后,再滴加BaCl2溶液才出现白色沉淀,该溶液中含有SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
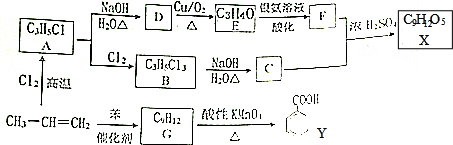
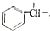 $→_{H+}^{KMnO_{4}}$
$→_{H+}^{KMnO_{4}}$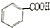
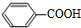 +CH2=CHCH2OH$→_{△}^{浓硫酸}$
+CH2=CHCH2OH$→_{△}^{浓硫酸}$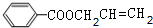 +H2O.
+H2O.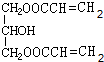 (任写一种即可).对于化合物X,下列说法正确的是AC.
(任写一种即可).对于化合物X,下列说法正确的是AC.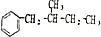 :则Z的同分异构体中,符合
:则Z的同分异构体中,符合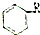 结构且有2个CH3的有3种(不包括Z).
结构且有2个CH3的有3种(不包括Z).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
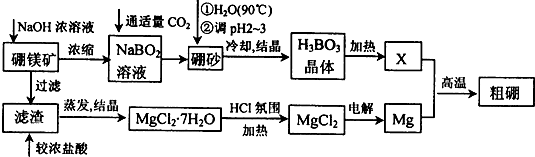
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 平衡常数K=$\frac{8}{3}$ | |
| B. | 达到平衡后NO2和SO2的转化率相等 | |
| C. | SO3和NO的体积比保持不变可以证明达到平衡状态 | |
| D. | 每消耗1molSO3的同时生成1molNO2可以证明达到平衡状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
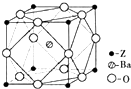 A、B、X、Y、Z为周期表前四周期元素,原子序数依次递增.已知:
A、B、X、Y、Z为周期表前四周期元素,原子序数依次递增.已知:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com