

| 2×3+2-4 |
| 2 |
| 2×3+2-4 |
| 2 |
| 浓硫酸 |
| △ |
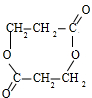 +2H2O,故答案为:2 HOCH2CH2COOH
+2H2O,故答案为:2 HOCH2CH2COOH| 浓硫酸 |
| △ |
 +2H2O;
+2H2O;

科目:高中化学 来源: 题型:
| A、电离平衡常数受溶液浓度的影响 | ||||
| B、电离常数大的酸溶液中c(H+)一定比电离常数小的酸溶液中的大 | ||||
| C、电离平衡常数可以表示弱电解质的相对强弱 | ||||
D、H2CO3的电离常数表达式:K=
|
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、一定只有C、H、O |
| B、可能含有C、H、O |
| C、一定含有C、H、无O |
| D、一定含有C、H、可能有O |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、两种难溶物质比较,溶度积小的溶解度不一定小 | ||||
| B、水的离子积常数KW随着温度的升高而增大,说明水的电离是放热反应 | ||||
C、向0.1mol/L的氨水中加入少量硫硫酸固体,则溶液中
| ||||
| D、0.1mol/L CH3COONa溶液中:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素符号 | X | Y | Z | M | N |
| 原子半径(nm) | 0.160 | 0.111 | 0.104 | 0.143 | 0.066 |
| 主要化合价 | +2 | +2 | -2,+4,+6 | +3 | -2 |
| A、单质与稀硫酸反应的速率快慢:M>Y>X |
| B、元素Z和N的质子数相差6 |
| C、元素Y和Z可能同周期 |
| D、相同条件下,等物质的量的单质与氢气化合放出能量的多少:N>Z |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(Na+ )+c(H+)═c(CH3COO- )+c(OH- ) |
| B、c(OH- )═c(H+ )+c(CH3COOH) |
| C、c(Na+ )=c(CH3COO- )+c(CH3COOH) |
| D、c(Na+ )>c(CH3COO- )>c(H+ )>c(OH- ) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com