
在某100 mL混合液中,HNO3和H2SO4的物质的量浓度分别是0.4 mol·L-1和0.1 mol·L-1。向该混合液中加入1.92 g铜粉,加热,待充分反应后,设溶液的体积仍为100 mL,则所得溶液中的Cu2+的物质的量浓度是( )
A.0.15 mol·L-1 B.0.225 mol·L-1 C.0.35 mol·L-1 D.0.45 mol·L-1
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
工业上常用FeCl3溶液腐蚀镀有铜的绝缘板生产印刷电路板,该反应的离子方程式为2Fe3++Cu=2Fe2++Cu2+。取上述反应后溶液20mL进行分析,测得其中c(Fe3+)为1mol/L,向其中加入足量的AgNO3溶液,生成沉淀 17.22g。则上述反应后20mL溶液中c(Cu2+)为
A.0.5 mol/L B.1mol/L C.1.5 mol/L D.2mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
据报道,某牙膏中含有的消毒剂三氯生,遇含氯的自来水会生成哥罗芳(三氯甲烷),哥罗芳能导致肝病,甚至癌症。已知三氯生的结构简式如右图所示,下列有关说法中不正确的是 ( )
A、三氯生能与NaOH反应
B、三氯生是一种芳香族化合物
C、三氯生与NaHCO3作用可产生CO2气体 D、哥罗芳没有同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
已知
| 共价键 | H—H | Cl—Cl | H—Cl |
| 键能/kJ·mol-1 | Q1 | Q2 | Q3 |
下列关系正确的是( )
A. Q1 +Q2>Q3 B.Q1 +Q2>2Q3 C. Q1 +Q2<Q3 D.Q1 +Q2<2Q3
查看答案和解析>>
科目:高中化学 来源: 题型:
某氮肥厂氨氮废水中氮元素多以 和NH3·H2O的形式存在,该废水的处理流程如下:
和NH3·H2O的形式存在,该废水的处理流程如下:


(1)过程Ⅰ:加NaOH溶液,调节pH至9后,升温至30 ℃,通空气将氨赶出并回收。用离子方程式表示加NaOH溶液的作用
(2)过程Ⅱ:在微生物作用的条件下, 经过两步反应被氧化成
经过两步反应被氧化成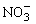 。两步反应的能量变化示意图如下:
。两步反应的能量变化示意图如下:

第一步反应是 反应(选填“放热”或“吸热”),判断依据是
。1 mol  (aq)完全转化成
(aq)完全转化成 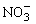 (aq)共与环境交换了 kJ热量。
(aq)共与环境交换了 kJ热量。
(3)过程Ⅲ:一定条件下,向废水中加入CH3OH,将HNO3还原成N2。若该反应消耗32 g CH3OH转移6 mol电子,则参加反应的还原剂和氧化剂的物质的量之比是
查看答案和解析>>
科目:高中化学 来源: 题型:
化学与生活密切相关,下列有关说法正确的是 ( )
A. 维生素C具有还原性,能在人体内起抗氧化作用
B. 糖类、蛋白质、油脂都属于天然高分子化合物
C. 煤经气化、液化和干馏三个物理变化过程,可变为清洁能源
D. 糖尿病人应少吃含糖类的食品,可常喝糯米八宝粥
查看答案和解析>>
科目:高中化学 来源: 题型:
等体积、等物质的量浓度的盐酸、氢氧化钠溶液分别放在甲、乙两烧杯中,各加等质量的铝,生成氢气的体积比为5:6(相同状况),则甲、乙两烧杯中的反应情况可能分别是
A.甲、乙中都是铝过量 B.甲中铝过量,乙中碱过量
C.甲中酸过量,乙中铝过量 D.甲中酸过量,乙中碱过量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com