
盐酸、硫酸和硝酸是中学阶段常见的“三大酸”。现就三大酸与金属铜反应的情况,回答下列问题:
(1)稀盐酸不与Cu反应,若在稀盐酸中加入H2O2(常见氧化剂,作氧化剂时还原产物为水)后,则可使铜顺利溶解。该反应的化学方程式为:____________________________________。
(2)在一定体积的10 mol·L-1的浓硫酸中加入过量铜片,加热使之反应,被还原的硫酸为0.9mol。则浓硫酸的实际体积_________(填“大于”、“等于”或“小于”)100ml。若使剩余的铜片继续溶解,可在其中加入硝酸盐溶液(如KNO3溶液),则该反应的离子方程式为
___________________________________________________________________________。
(3)根据下图操作及现象推断酸X为______________(填选项)。
a、浓盐酸 b、浓硫酸 c、浓硝酸

 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案科目:高中化学 来源: 题型:
霉酚酸是一种生物活性化合物,如右图。下列有关霉酚酸的说法正确的是 ( )
A.分子式为:C17H18O6
B.处于同一平面的碳原子至多9个
C.不能与FeCl3溶液发生显色反应
D.一定条件下 1 mol霉酚酸最多可与3 mol NaOH反应

查看答案和解析>>
科目:高中化学 来源: 题型:
向NaI和NaBr的混合溶液中通入足量的氯气,充分反应后将溶液蒸干,灼烧上述残留物,最后得到的物质是
A.NaCl、I2 B.NaCl、NaBr C.NaBr、I2 D.NaCl
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应的离子方程式正确的是
A.NaHCO3溶液与盐酸:CO32− + 2 H+ = H2O + CO2↑
B.硝酸银溶液与铜:Cu + Ag+ = Cu2+ + Ag
C.向硝酸亚铁溶液中加入稀硫酸:Fe2++4H++NO3-=Fe3++NO↑+2H2O
D.用醋酸除水垢:2CH3COOH + CaCO3 = Ca2+ + 2CH3COO− + H2O + CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
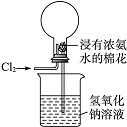
下图是模拟氯碱工业生产中检查氯气是否泄漏的装置,下列有关说法错误的是
A.烧瓶中立即出现白烟
B.烧瓶中立即出现红棕色
C.烧瓶中发生的反应表明常温下氨气有还原性
D.烧杯中的溶液是为了吸收有害气体
查看答案和解析>>
科目:高中化学 来源: 题型:
化学与生活、环境密切相关,下列说法错误的是
A.粮食酿造的酒一定温度下密封存放时间越长香味越浓,是因为有酯生成
B.纤维素在人体内可水解为葡萄糖,故可直接成为人类的营养物质
C.用纯碱制玻璃、用铁矿石炼铁、用淀粉发酵法生产酒精都会产生CO2
D.用浸泡过高锰酸钾溶液的硅藻土吸收水果释放的乙烯,可达到水果保鲜的目的
查看答案和解析>>
科目:高中化学 来源: 题型:
能源的开发、利用与人类社会的可持续发展息息相关,怎样充分利用好能源是摆在人类面前的重大课题。
I.已知:Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g)△H= a kJ•mol-1
CO(g)+1/2O2(g)=CO2(g)△H= b kJ•mol-1
C(石墨)+O2(g)=CO2(g)△H= c kJ•mol-1
则反应:4Fe(s)+3O2(g)=2Fe2O3(s)的焓变△H= kJ•mol-1
Ⅱ.(1)依据原电池的构成原理,下列化学反应在理论上可以设计成原电池的是
A.C(s)+CO2(g)= 2CO(g)
B.NaOH(aq)+HCl(aq)= NaCl(aq)+H2O(l)
C.2H2O(l)= 2H2(g)+O2(g)
D.CH4(g)+2O2(g)= CO2(g)+2H2O(l)
若以KOH溶液为电解质溶液,依据所选反应可以设计成一个原电池,请写出该原电池的电极反应
负极:
正极:
 (2)二氧化氯(ClO2)是一种高效安全的自来水消毒剂。ClO2是一种黄绿色气体,易溶于水.实验室以NH4Cl、盐酸、NaClO2为原料制备ClO2流程如下:
(2)二氧化氯(ClO2)是一种高效安全的自来水消毒剂。ClO2是一种黄绿色气体,易溶于水.实验室以NH4Cl、盐酸、NaClO2为原料制备ClO2流程如下:
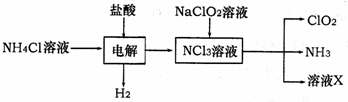
已知:电解过程中发生的反应为:
NH4Cl+2HCl NCl3+3H2↑;假设NCl3中氮元素为+3价.
①写出电解时阴极的电极反应式
阳极的电极反应式
②在阳极上放电的物质(或离子)是
③除去ClO2中的NH3可选用的试剂是 (填序号)
A.生石灰 B.碱石灰 C.浓H2SO4 D.水
④在生产过程中,每生成1mol ClO2,需消耗 mol NCl3.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com