
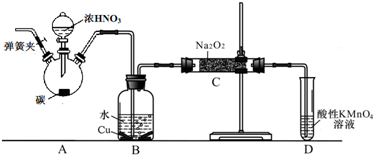
���� ��1��װ��A����Ũ�����̼���ȷ����ķ�Ӧ����Ӧ���ɶ��������Ͷ�����̼��ˮ������������ԭ��Ӧ�����غ�� ԭ���غ���ƽ��
��2��װ��B����Aװ�����ɵĶ���������ˮ��Ӧ���������һ�������������ͭ��Ӧ��������ͭ��һ��������ˮ��ͨ��װ��C�еĹ�����������һ��������������̼�����ͨ�����Ը��������Һ��ȥʣ��һ��������ֹ��Ⱦ������
��3�������������ƾ��������Ի�ԭ�ԣ�ѡ��ԭ���������������ķ�Ӧ����֤���������Ƿ����������ƣ�
��4��a������̼���Ƶķ�Ӧ�Ƕ�����̼�������Ʒ����ķ�Ӧ������̼���ƺ�������
b��Ϊ����װ���еĿ������²�Ʒ��������Ҫ���ɼ�ͨ�뵪���ž�װ���еĿ�����
��5�������������Ƶ����ʷ���������������ǿ�������Σ�
a����������Ϊ��ɫ������ɫ��ĩ�����״��ζ�̣�������ˮ����ۼ���ζ����ʳ�����ƣ����ڹ�ҵ������ҵ�й�Ϊʹ�ã�������Ʒ��Ҳ������Ϊ��ɫ������ʹ�ã���������������ʳ���ж��Ļ��ʽϸߣ�
b��0.1mol/L��������Һ����������ڵ���ƽ�������
c��������Һ�е���غ�����жϣ�
d�����������������ˮ���Լ��Է�������Ũ�ȴ�С��
��� �⣺��1��װ��A����Ũ�����̼���ȷ���Ӧ����Ӧ���ɶ��������Ͷ�����̼��ˮ����Ӧ�Ļ�ѧ����ʽΪC+4HNO3��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CO2��+4NO2��+2H2O��
�ʴ�Ϊ��C+4HNO3��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CO2��+4NO2��+2H2O��
��2��װ��B����Aװ�����ɵĶ���������ˮ��Ӧ���������һ��������3NO2+H2O=2HNO3+NO�������ͭ��Ӧ��������ͭ��һ��������ˮ�����Է�Ӧ����Ϊ��Һ������ͭƬ�ܽ⣬���ܿ�����ɫ����ð����ͨ��װ��C�еĹ�����������һ��������������̼�����ͨ�����Ը��������Һ��ȥʣ��һ��������ֹ��Ⱦ������
�ʴ�Ϊ����Һ������ͭƬ�ܽ⣬���ܿ�����ɫ����ð������ȥδ��Ӧ��NO����ֹ��Ⱦ������
��3�������������Ƶ�ʵ�����Ϊ�������������Թ��У�����ϡ���ᣬ��������ɫ���岢��Һ���Ϸ���Ϊ����ɫ����D�в������������ƣ���Ӧ�����ӷ���ʽ��3NO2-+2H+=NO3-+2NO��+H2O��
�������������Թ��У���������KMnO4��Һ������Һ��ɫ��ȥ����D�в������������ƣ���Ӧ�����ӷ���ʽ��5NO2-+2MnO4-+6H+=5NO3-+2Mn2++3H2O��
�ʴ�Ϊ���������������Թ��У�����ϡ���ᣬ��������ɫ���岢��Һ���Ϸ���Ϊ����ɫ����D�в������������ƣ�
��4��a������̼���Ƶķ�Ӧ�Ƕ�����̼�������Ʒ����ķ�Ӧ����Ӧ�Ļ�ѧ����ʽΪ��2CO2+2Na2O2�T2Na2CO3+O2��ͨ��װ��C�еĹ�����������һ��������������̼��һ����������Ⱦ�����壬���ͨ�����Ը��������Һ��ȥʣ��һ��������ֹ��Ⱦ������Ϊ�ų�������B��Cװ�ü�����װ��E��E��ʢ�ŵ��Լ�Ӧ��ʯ�ң��������ն�����̼��
�ʴ�Ϊ��2CO2+2Na2O2�T2Na2CO3+O2����ʯ�ң�
b��Ϊ����װ���еĿ������²�Ʒ��������Ҫ���ɼ�ͨ�뵪���ž�װ���еĿ�����
�ʴ�Ϊ�����ɼУ�ͨ��N2һ��ʱ�䣻
��5��a����������Ϊ��ɫ������ɫ��ĩ�����״��ζ�̣�������ˮ����ۼ���ζ����ʳ�����ƣ����ڹ�ҵ������ҵ�й�Ϊʹ�ã�������Ʒ��Ҳ������Ϊ��ɫ������ʹ�ã���������������ʳ���ж��Ļ��ʽϸߣ����Բ�����������ʳ��ʳ�ã���a����
b��0.1mol/L��������Һ����������������ڵ���ƽ�⣬���Գ����£�0.1mol/L��������ҺpH��1����b��ȷ��
c��������Һ�е���غ������.1mol/L����������Һ�д��ڣ�c��Na+��+c��H+��=c��NO2-��+c��OH-������c��ȷ��
d�����������������ˮ���Լ��Է�������Ũ�ȴ�С��0.1mol/L����������Һ�д��ڣ�c��Na+����c��NO2-����c��OH-����c��H+������d����
�ʴ�Ϊ��bc��
���� ���⿼���������Ʊ�ʵ�鷽������ƺ���Ϣ�жϣ��������ʵ�����Ӧ�ã�ע��ʵ������еķ�Ӧ������������ջ����ǹؼ�����Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ��Ӧʱ��/min | 0 | 5 | 10 | 15 | 20 | 25 |
| ѹǿ/MPa | 12.6 | 10.8 | 9.5 | 8.7 | 8.4 | 8.4 |
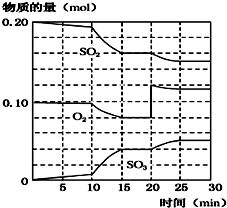
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
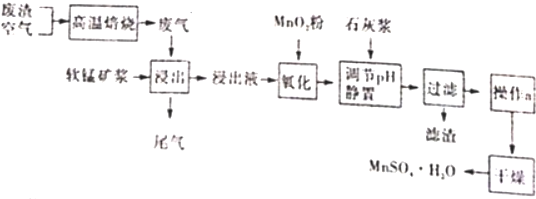
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
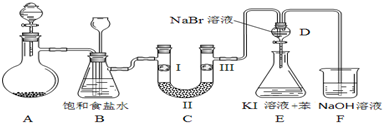
| a | b | c | d | |
| I | �������ɫ���� | �������ɫ���� | ʪ�����ɫ���� | ʪ�����ɫ���� |
| �� | ��ʯ�� | �轺 | Ũ���� | ��ˮ�Ȼ��� |
| �� | ʪ�����ɫ���� | ʪ�����ɫ���� | �������ɫ���� | �������ɫ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ִ�ˮ�����µĴ�����װһ��������п�� | |
| B�� | ��п�����ȶ����������� | |
| C�� | ��п��ϡ���ᷴӦʱ��������������ͭ��Һ�����ʼӿ� | |
| D�� | ���ƽ��ƾ��ú����䰵 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���������ʯ���Ӷ�����������ṹ | |
| B�� | �����ζ�������ˮ? | |
| C�� | �����ᡢ����ܷ�����Ӧ | |
| D�� | ԭ��������Ӧ���������Ƕ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
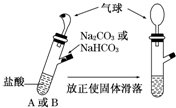
| A�� | Aװ�õ����������ٶȿ� | |
| B�� | �����������������ͬ���������Ũ��һ�����ڻ����2 mol/L | |
| C�� | �����������������ͬ���������Ũ��һ��С�ڻ����1 mol/L | |
| D�� | �������Թ���Na+�����ʵ���һ����ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | B��C��A��D | B�� | A��C��D��B | C�� | D��A��C��B | D�� | C��D��A��B |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����Һ�м�������KCl���壬��Һ��ɫ��dz | |
| B�� | �����¶ȣ�ƽ��һ�������ƶ� | |
| C�� | ��������KCl�������������FeCl3����ƽ�ⳣ���������仯���ұ仯�����෴ | |
| D�� | ƽ�ⳣ������ʽΪK=$\frac{c[Fe��SCN��_{3}]•{c}^{3}��KCl��}{c��FeC{l}_{3}��•{c}^{3}��KSCN��}$ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com