
| A、MgO、Al2O3的熔点很高,可制作耐高温材料,工业上也用其电解冶炼对应的金属 |
| B、明矾水解形成的胶体能吸附水中悬浮物,可用于水的净化 |
| C、燃放的焰火是某些金属元素焰色反应所呈现出来的色彩 |
| D、铝比铁活泼,但铝制品比铁制品在空气中耐腐蚀 |


科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氢气在氯气中燃烧发出苍白色火焰,在瓶口有白雾生成 |
| B、红热的铜丝在氯气中剧烈燃烧,生成棕黄色的烟,加入少量水形成蓝色溶液 |
| C、金属Na在氯气中燃烧产生淡黄色的烟 |
| D、红热的铁丝在氯气中燃烧产生红棕色的烟 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、7种 | B、8 种 |
| C、9种 | D、10种 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、金属晶体具有良好的延展性,是因为金属晶体中的原子层在滑动过程中金属键未破坏 |
| B、电子云图象中黑点的疏密是指电子数的多少 |
| C、含有极性键的分子一定是极性分子 |
| D、键能越大,表示该分子越容易受热分解 |
查看答案和解析>>
科目:高中化学 来源: 题型:

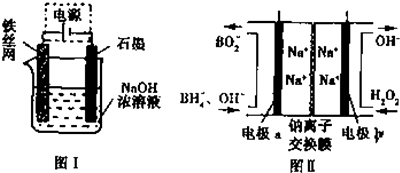
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、[Cr(H2O)6]Cl3 |
| B、[Cr(H2O)5Cl]Cl2 |
| C、[Cr(H2O)4Cl2]Cl |
| D、[Cr(H2O)3Cl3] |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、难溶电解质的Ksp越小,溶解度就一定越小 |
| B、一般认为沉淀离子浓度小于1.0×10-5 mol/L时,沉淀就达完全 |
| C、用饱和Na2CO3溶液可以将BaSO4转化为BaCO3,说明Ksp(BaCO3)小于Ksp(BaSO4) |
| D、向含AgCl沉淀的悬浊液中加入NaCl饱和溶液,AgCl的溶解度变小,溶度积常数变小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com