
����Ŀ����Ũ����ȡ������Ϊ50mL��A��B����NaOH��Һ�У���ͨ��һ������CO2����ϡ�͵�100mL����ϡ�ͺ����Һ����μ���0.1mol/L�����ᣬ����CO2���������״��������������������ϵ����ͼ��ʾ��
��A���߱�����ԭ��Һͨ��CO2���������������ᷴӦ����CO2����������mL����״������
��B���߱�����ԭ��Һͨ��CO2��������Һ�����ʵĻ�ѧʽΪ���ʵ���֮��Ϊ��
��ԭNaOH��Һ�����ʵ���Ũ��Ϊ ��
���𰸡�112��Na2CO3��NaHCO3��1��1��0.15mol/L
���������⣺��ͼ��֪����ӦB��Һ��˵���μ�����60mLʱû���������ɣ����ܷ���OH��+H+=H2O��CO32��+H+=HCO3�� �� ����ԭ��Һ��ֻ��̼���ƣ�����̼��������Ҫ����������̼�����������Ȼ�����Ҫ����������ȣ�ʵ������Ҫ��������60mLԶԶ����̼�����������Ȼ�����Ҫ����������75��60��mL=15mL��˵��ԭ��Һ�е�������NaOH��Na2CO3������A��Һ��˵���μ�����25mLʱû���������ɣ����ܷ���OH��+H+=H2O��CO32��+H+=HCO3�� �� ����ԭ��Һ��ֻ��̼���ƣ�����̼��������Ҫ����������̼�����������Ȼ�����Ҫ����������ȣ�ʵ������Ҫ��������25mLС��̼�����������Ȼ�����Ҫ����������75��25��mL=50mL��˵��ԭ��Һ�е�������Na2CO3��NaHCO3 �� �ٶ���A��Һ��˵���μ�����25mLʱ���������ɣ���μ���0.1molL��1 �����ᣬ������CO2����ʱ��������ӦHCO3��+H+=H2O+CO2������HCO3��+H+=H2O+CO2��
11
n��CO2��=0.05L��0.1mol/L=0.005mol����������Ϊ0.005mol��22.4L/mol=0.112L=112mL��
���Դ��ǣ�112��
��������������֪��B��������Na2CO3��NaHCO3 �� ����������Ĺ�ϵ��֪�����ߵ����ʵ�����ͬ�������ʵ�����Ϊ1��1�����Դ��ǣ�Na2CO3��NaHCO3��1��1���ۼ�����������������Һ�о�ֻ����NaCl��n��HCl��=n��NaOH��=0.075L��0.1mol/L=0.0075mol��c��NaOH��= ![]() =
= ![]() =0.15mol/L��
=0.15mol/L��
���Դ��ǣ�0.15mol/L��


 ��ǰ����ϵ�д�
��ǰ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������Ϊ�����Ʊ�������������Һ������������
A. þ��B. п��C. ��ƬD. ͭƬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����º����£���2mol����A��2mol����Bͨ�����Ϊ2L���ܱ������У��������·�Ӧ��2A(g)+B(g)![]() xC(g)+2D(s)��2min��Ӧ�ﵽƽ��״̬����ʱʣ��1.2mol B�������C��Ũ��Ϊ1.2mol/L��
xC(g)+2D(s)��2min��Ӧ�ﵽƽ��״̬����ʱʣ��1.2mol B�������C��Ũ��Ϊ1.2mol/L��
��1���ӿ�ʼ��Ӧ��ƽ��״̬������C��ƽ����Ӧ����Ϊ__________��
��2��x=_________���÷�Ӧ�Ļ�ѧƽ�����ʽΪ________________��
��3��A��ת������B��ת����֮��Ϊ________��
��4�����и������Ϊ�÷�Ӧ�ﵽƽ��״̬�ı�־��_______������ĸ����
A��ѹǿ���ٱ仯 B�������ܶȲ��ٱ仯
C������ƽ����Է����������ٱ仯 D��A������������B����������֮��Ϊ2:1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Һ��X2O72-��SO32-��������֮��Ϊ1��3ʱ������ȫ����������ԭ��Ӧ��X�ڻ�ԭ�����еĻ��ϼ�Ϊ
A. +1 B. +2 C. +3 D. +4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʾ�����������ڴ����а���ȼ�ա�����ijУ��ѧС��ѧ���������װ�ã�ͼ�����еȼг�װ������ȥ�����а����������ڲ�ͬ�����·�Ӧ��ʵ�飮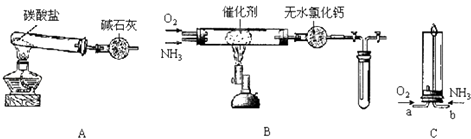
�ش��������⣮
��1����װ��A��ȡ����������İ��������Թ���̼���εĻ�ѧʽ������ʯ�ҵ������� ��
��2���������İ��������������ͨ��װ��B������Ϊ��ʯ�ޣ��У��þƾ���Ƽ��ȣ��ٰ��������Ļ�ѧ����ʽ����
���Թ��������Ϊ����ɫ���÷�Ӧ�Ļ�ѧ����ʽ�� ��
��3����������������A�����İ����ֱ��a��b���ܽ�����ͨ�뵽װ��C�У�����b���϶˵�ȼ�������ɹ۲쵽��������ȼ�գ�������������������������ͨ����Ⱥ�˳���� �� �������� ��
����ʵ�������֪������ȼ�յĻ�ѧ����ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijУ��ѧ�о���ѧϰС�������ʵ����֤Fe��Cu�Ľ�����ԣ�����������������ַ��������������������й�ʵ����Ŀ��
�����������������С��ȵ���Ƭ��ͭƬ���ֱ�ͬʱ����ϡ�����ϡ�����У��۲�������ݵĿ������ݴ�ȷ�����ǵĻ�ԣ���ԭ�������ӷ���ʽΪ ��
��������������Fe��Cu���缫��Ƴ�ԭ��أ���ȷ�����ǵĻ�ԣ���������ķ����ڻ���ԭ���װ��ͼ�����ԭ��صĵ缫���Ϻ͵������Һ��
��д���缫��Ӧʽ��������Ӧʽ����������Ӧʽ����
�����������ѧ��֪ʶ���������������һ����֤Fe��Cu��Եļ�ʵ�鷽���뷽��������ͬ�� �� �����ӷ���ʽ��ʾ�䷴Ӧԭ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ȡ����ͭ������ʾ��ͼ����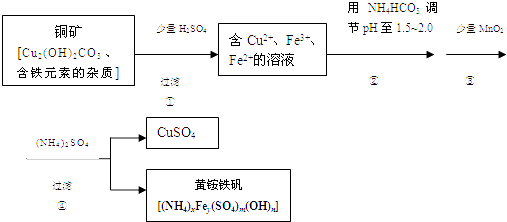
��1���������Cu2��OH��2CO3 ������Ӧ�Ļ�ѧ����ʽΪ ��
��2���ڲ���۷����ķ�Ӧ�У�1mol MnO2ת��2mol ���ӣ��÷�Ӧ�����ӷ���ʽΪ ��
��3����С��Ϊ�ⶨ�����������ɣ�����������ʵ�飺a����ȡ4.800g��Ʒ����������ȫ�ܽ�����100.00mL��ҺA��
b����ȡ25.00mL��ҺA������������KI����0.2500molL��1Na2S2O3��Һ���еζ�����Ӧ����ʽΪI2+2Na2S2O3=2NaI+Na2S4O6��������30.00mLNa2S2O3��Һ���յ㣮
b����ȡ25.00mL��ҺA������������NaOH��Һ��ַ�Ӧ���ˡ�ϴ�ӡ����յú�ɫ��ĩ0.600g��
c����ȡ25.00mL��ҺA��������BaCl2��Һ��ַ�Ӧ���ˡ�ϴ�ӡ�����ó���1.165g��
����Na2S2O3��Һ���еζ�ʱ���ζ����յ����ɫ�仯Ϊ �� ��
��ͨ������ȷ����������Ļ�ѧʽ��д��������̣���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ�������ܡ����ܵ����ת�������ڻ�ѧ�������������ת����˵����ȷ���ǣ� �� 
A.��ѧ��Ӧ�������仯����Ҫԭ���ǻ�ѧ���Ķ���������
B.���ȷ�Ӧ�У���Ӧ��������������������������
C.ͼI��ʾ��װ���ܽ���ѧ��ת��Ϊ����
D.ͼII��ʾ�ķ�ӦΪ���ȷ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ʵ�����Fe��Mg��Al�ֱ������������ʵ���Ũ����ͬ��������ȫ��Ӧ����������������Ϊ�� ��
A.2��3��1
B.2��2��3
C.3��2��1
D.1��3��2
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com