
| A. | 化学变化过程中一定伴随着能量变化 | |
| B. | 放热反应可能需要加热才能进行 | |
| C. | 吸热反应只能在加热条件下才能进行 | |
| D. | 天然气在空气中燃烧时,能量转化形式不止一种 |
分析 A.化学反应的实质为旧键的断裂和新键的形成,化学键的断裂和形成伴随着能量变化;
B.反应是否加热才能进行与反应热无关;
C.氢氧化钡晶体与氯化铵的反应,为吸热反应,常温下可进行;
D.燃烧时,化学能可转化为热能、光能等.
解答 解:A.化学反应的实质为旧键的断裂和新键的形成,化学键的断裂吸收能量,形成化学键放出能量,则一定伴随着能量变化,故A正确;
B.有些放热反应需要在加热条件下进行,如铝热反应等,也有些放热反应常温下就可进行,如中和反应等,故B正确;
C.氢氧化钡晶体与氯化铵的反应,为吸热反应,常温下可进行,则吸热反应不一定需要加热,故C错误;
D.天然气在空气中燃烧时,发光发热,则化学能可转化为热能、光能等.故D正确;
故选C.
点评 本题综合考查化学反应与能量变化,为高频考点,侧重考查学生的分析能力,注意把握常见吸热反应、放热反应的特点,把握能量转化的形式,难度不大.


科目:高中化学 来源: 题型:实验题
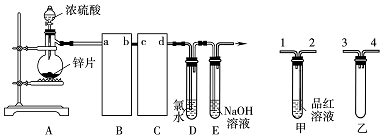
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
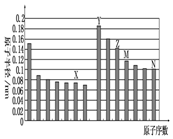
| A. | Z、N两种元素形成的化合物熔融状态下可以导电 | |
| B. | X、N两种元素的气态氢化物的沸点相比,前者较低 | |
| C. | Z的氧化物能分别溶解于Y的氢氧化物和N的氢化物的水溶液中 | |
| D. | 由X与M两种元素组成的化合物能与水反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 键长越长,键能越小,共价化合物越稳定 | |
| B. | 通过反应物和生成物分子中键能数据可以粗略预测反应热的大小 | |
| C. | 键角是确定多分子立体结构(分子形状)的重要参数 | |
| D. | 同种原子间形成的共价键键长长短总是遵循:叁键<双键<单键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
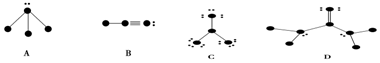
 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在放电时,两极质量均增加 | |
| B. | 在充电时,电池中硫酸的浓度不断变小 | |
| C. | 在放电时,负极发生的反应是 Pb+2e-+SO42-=PbSO4 | |
| D. | 在放电时,正极发生的反应是 PbSO4+2e-=Pb+SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 ),其原理如下图所示,下列说法正确的是( )
),其原理如下图所示,下列说法正确的是( )
| A. | A极的电极反应式为  +e-=Cl-+ +e-=Cl-+ | |
| B. | 当外电路中有0.2mole-转移时,A极区增加的H+的个数为0.1NA | |
| C. | 电流方向从B极沿导线经小灯泡流向A极 | |
| D. | B为电池的正极,发生还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10% | B. | 30% | C. | 50% | D. | 70% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 物质 | X | Y | Z |
| 初始浓度(mol•L-1) | 0.1 | 0.2 | 0 |
| 平衡浓度(mol•L-1) | 0.05 | 0.05 | 0.1 |
| A. | 反应可表示为X+3Y?2Z,其平衡常数为1600 | |
| B. | 增大压强使平衡向生成Z的方向移动,平衡常数增大 | |
| C. | 反应达到平衡时,X的转化率为50% | |
| D. | 反应起始时和达平衡时的压强比为3:2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com