
【题目】U、V、W、X、Y、Z是原子序数依次增大的短周期元素。已知:
①WU4++XU-==WU3+U2X,各种反应物和生成物的电子总数都与Y+相等;
②Z的单质在X2中燃烧的产物可使品红溶液褪色;
③V的单质在X2中燃烧可生成VX和VX2两种气体;
④Y的单质是一种金属,该金属与X2反应可生成Y2X和Y2X2两种固体。
请回答下列问题:
(1)写出Y2X2与水反应的化学方程式:________________。
(2)V、W、X形成的10电子氢化物中,沸点最高的是__________(写化学式)。
(3)U2X2与FeSO4按物质的量之比1:2溶于稀硫酸中,反应的离子方程式为__________。
(4)常温下,向pH=11的Y2VX3溶液中加入过量石灰乳,过滤后所得溶液pH=13,则反应前的溶液中与反应后的滤液中水电离出的c(OH-)的比值是_________。
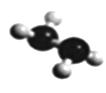
(5)已知由U、W两种元素组成的共价化合物联氨的球棍模型如图所示,则联氨分子的电子式为____________。联氨为二元弱碱,在水中的电离方程式与氨相似,联氨第一步电离反应的平衡常数值为_______(已知:N2H4+H+==N2H5+的K=8.7×107;KW=1.0×10-14)。联氨与过量硫酸形成的酸式盐的化学式为______________。
【答案】 2Na2O2+2H2O=4NaOH+O2↑ H2O H2O2+2Fe2++2H+=2Fe3++2H2O 1×1010 ![]() 8.7×10-7 N2H6(HSO4)2
8.7×10-7 N2H6(HSO4)2
【解析】本题考查元素的推断,①根据化学反应方程式,推出此反应式NH4++OH-=NH3+H2O,都含有10个电子,即Y为Na;②Z的单质在O2中燃烧的产物可使品红溶液褪色,即产物是SO2,即Z为S;③V的单质在氧气燃烧可生成VX和VX2,即V为C,(1)Y2X2为Na2O2,与水反应的化学方程式为2Na2O+2H2O=4NaOH+O2↑;(2)氢化物分别是CH4、NH3、H2O,H2O、NH3存在分子间氢键,CH4中没有,因此CH4的沸点最低,NH3和H2O中H2O的相对分子质量最大,即H2O的沸点大于NH3,H2O的沸点最高;(3)是H2O2与FeSO4的反应,利用H2O2的氧化性把Fe2+氧化成Fe3+,即离子反应式为H2O2+2Fe2++2H+=2H2O+2Fe3+;(4)Y2VX3的化学式为Na2CO3,pH=11的Na2CO3溶液中,由水电离c(OH-)=Kw/c(H+)=10-14/10-11mol·L-1=10-3mol·L-1,加入石灰乳后得到溶液为NaOH,此时溶液中水电离c(OH-)=c(H+)=10-13mol·L-1,因此两者比值为10-3/10-13=103:1;(5)组成的分子式为N2H4,其电子式为:![]() ;联氨为二元弱碱,在水中的电离方程式与氨相似,则联氨第一步电离的方程式为N2H4+H2O
;联氨为二元弱碱,在水中的电离方程式与氨相似,则联氨第一步电离的方程式为N2H4+H2O![]() N2H5++OH-,平衡常数K1=c(N2H5+)×c(OH-)/c(N2H4)=K×Kw8.7×107×1×10-14=8.7×10-7;联氨为二元弱碱,酸碱发生中和反应生成盐,则联氨与过量硫酸形成酸式盐的化学式为N2H6(HSO4)2 。
N2H5++OH-,平衡常数K1=c(N2H5+)×c(OH-)/c(N2H4)=K×Kw8.7×107×1×10-14=8.7×10-7;联氨为二元弱碱,酸碱发生中和反应生成盐,则联氨与过量硫酸形成酸式盐的化学式为N2H6(HSO4)2 。


 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案科目:高中化学 来源: 题型:
【题目】某无色透明溶液能与铝粉反应放出H2,则此溶液中一定能大量共存的离子组是( )
A.Na+ Cl- CO32- Cu2+ B.Na+ Cl- K+ SO42-
C.SO42- Mg2+ Ba2+ Cl- D.Na+ Cl- K+ HCO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】100℃时,将0.1 mol N2O4置于1L密闭的烧瓶中,然后将烧瓶放入100℃ 的恒温槽中,烧瓶内的气体逐渐变为红棕色:N2O4(g) ![]() 2NO2 (g)。下列结论不能说明上述反应在该条件下已经达到平衡状态的是
2NO2 (g)。下列结论不能说明上述反应在该条件下已经达到平衡状态的是
①N2O4的消耗速率与NO2的生成速率之比为1:2 ;②NO2生成速率与NO2消耗速率相等;③烧瓶内气体的压强不再变化;④烧瓶内气体的质量不再变化;⑤NO2的物质的量浓度不再改变;⑥烧瓶内气体的颜色不再加深;⑦烧瓶内气体的平均相对分子质量不再变化;⑧烧瓶内气体的密度不再变化。
A.②③⑥⑦ B.①④⑧ C.只有①④ D.只有⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题:
(1)写出泡沫灭火器的灭火原理的离子方程式
(2)已知25℃,101 kPa时:
S(s)+O2(g)==SO2(g) H=-296.8 kJ/mol
2Cu(s)+O2(g)==2CuO(s) H=-314.6 kJ/mol
Cu(s)+S(s)==CuS(s) H=-53.1 kJ/mol
写出CuS(s)与O2(g)反应生成CuO(s)和SO2(g)的热化学方程式 。
(3)已知常温下AI(OH)3的Ksp=l.0×10-33,若溶液中c(Al3+)为1.0 mol/L,请计算Al3+开始沉淀的pH= 。常温下,浓度均为0.01mol/L的CH3COOH和CH3COONa的混合液中,PH = a,则醋酸的电离常数约为Ka = 。
(4)在常温下,向V L pH=12的Ba(OH)2溶液中逐滴加入一定浓度的NaHSO4稀溶液,当溶液中的Ba2+ 恰好沉淀完全时,溶液pH=11。则Ba(OH)2溶液与NaHSO4溶液的体积比为 ,NaHSO4溶液的物质的量浓度为 mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g),在5 L密闭容器中进行,半分钟后,NO的物质的量增加了0.3 mol,则此反应的平均速率为( )
4NO(g)+6H2O(g),在5 L密闭容器中进行,半分钟后,NO的物质的量增加了0.3 mol,则此反应的平均速率为( )
A. v(O2)=0.01 mol/(L·s) B. v(NO)=0.008 mol/(L·s)
C. v(H2O)=0.003 mol/(L·s) D. v(NH3)=0.004 mol/(L·s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的数值,下列说法正确的是( )
A.2.4gMg与足量盐酸反应失去0.2NA个电子
B.标准状况下,22.4L水中含有NA个H2O分子
C.1 mol·L-1 Na2CO3溶液中有2NA个Na+
D.78gNa2O2与足量的水反应转移电子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关除杂质(括号中为杂质)的操作中,正确的是
A. 甲烷(乙烯):通入足量酸性高锰酸钾溶液洗气
B. 硝基苯(硝酸):多次加入氢氧化钠溶液,充分振荡,分液,弃水层
C. 溴苯(漠):加水振荡,分液,弃水层
D. 乙酸乙酯(乙酸):加饱和碳酸钠溶液,蒸馏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在无色透明酸性溶液中,能共存的离子组是
A.NH4+、OH-、Al3+、Cl- B.K+、SO42-、HCO3-、Na+
C.Mg2+、NO3-、Cl-、Na+ D.MnO4-、K+、SO42-、Na+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com