
| 6.72L |
| 22.4L/mol |
| 5.4g |
| 27g/mol |
| 6.72L |
| 22.4L/mol |
| 5.4g |
| 27g/mol |
| ||
| ||



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Na2CO3=Na22++CO32- |
| B��NaHSO4=Na++H++SO42- |
| C��CH3COOH=H++CH3COO- |
| D��H2CO3=2H++CO32- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
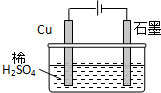
| A���������У�ͭ�缫����H2���� | ||||
| B�����һ��ʱ���ʯī�缫����H2���� | ||||
| C�������������У�H+��Ũ�Ȳ������� | ||||
D�������ڣ�����Ӧ����ʽΪ��Cu+H2SO4
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
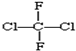 ��
��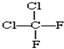 �� ��
�� ��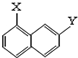 ��
��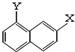 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
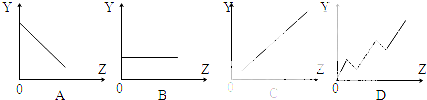
| Ԫ�ش��� | L | M | Q | R | T |
| ԭ�Ӱ뾶/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 |
| ��Ҫ���ϼ� | +2 | +3 | +6��-2 | +2 | -2 |
| Ԫ�ش��� | Ԫ��������Ϣ |
| A | �䵥�����ܶ���С�����ʣ� |
| B | �����Ӵ�������λ����ɣ������ǿ�������Ҫ�ɷ�֮һ�� |
| C | ����������B������������ͬ�ĵ��Ӳ�ṹ������BԪ�ؿ����γ��������ϵ����ӻ���� |
| D | ����������������ﶼ�����ԣ���Cͬ���� |
| E | ��Cͬ���ڣ�ԭ�Ӱ뾶�ڸ�������С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����ǵؿ��к�������Ԫ�� |
| B�������⻯��ȼ��⻯�����ȶ���ǿ |
| C��������γɵĻ�������������ά |
| D���ס�������Ԫ���γɵĻ������п��ܼȺ����Ӽ��ֺ��й��ۼ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ȡ100mL5mol/LH2SO4������400mLˮ |
| B��ȡ200mL5mol/LHCl����ˮϡ����500mL |
| C��ȡ100 mL5mol/LH2SO4����ˮ500mL |
| D��ȡ100 mL5mol/LHNO3����ˮϡ����500mL |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�������ӵ�������һ��������û�е�λ |
| B������NA��ʾ�����ӵ����� |
| C�������ӵ�������һ��ʵ��ֵ |
| D�������ӵ��������ã�6.02��1023mol-1 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com