
分析 二氧化硫和氯气在水溶液中反应生成硫酸和盐酸,硫酸根和钡离子反应生成硫酸钡沉淀;二氧化硫和氨水反应生成亚硫酸铵,亚硫酸根和钡离子反应生成亚硫酸钡沉淀;
解答 解:二氧化硫和氨水反应生成亚硫酸铵,反应的离子方程式为:SO2+2NH3•H2O=2NH4++SO32-+H2O,亚硫酸根和钡离子反应生成亚硫酸钡沉淀,反应的离子方程式为:SO32-+Ba2+═BaSO3↓,离子方程式可以写成:Ba2++2NH3•H2O+SO2=BaSO3↓+2NH4++H2O,二氧化硫和氯气在水溶液中反应生成硫酸和盐酸,反应的离子方程式为:SO2+Cl2+2H2O═4H++2Cl-+SO42-,硫酸根和钡离子反应生成硫酸钡沉淀,SO42-+Ba2+═BaSO4↓,离子方程式可以写成:Ba2++Cl2+SO2+2H2O=BaSO4↓+4H++2Cl-,该沉淀的成分分别为BaSO3,BaSO4,
故答案为:BaSO3,BaSO4,Ba2++2NH3•H2O+SO2=BaSO3↓+2NH4++H2O,Ba2++Cl2+SO2+2H2O=BaSO4↓+4H++2Cl-;
点评 本题考查了二氧化硫的性质分析,主要是二氧化硫的还原性和酸性氧化物性质的理解应用和离子方程式书写方法,题目较简单.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 100℃时,pH=10的NaOH溶液和pH=2的H2SO4恰好中和,所得溶液的pH=7 | |
| B. | 25℃时,0.2 mol/L Ba(OH)2溶液和0.2 mol/L HCl等体积混合,所得溶液的pH=7 | |
| C. | 25℃时,0.2 mol/L NaOH溶液与0.2 mol/L H2SO4恰好中和,所得溶液的pH<7 | |
| D. | 25℃时,pH=12的氨水和pH=2的H2SO4等体积混合,所得溶液的pH>7 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | KClO3和SO2溶于水后的溶液均可导电,故KClO3和SO2均为电解质 | |
| B. | CH3COOH溶液加水稀释后,溶液中$\frac{c(C{H}_{3}COOH)}{c(C{H}_{3}CO{O}^{-})}$的值增大 | |
| C. | 反应NH3(g)+HCl(g)=NH4Cl(s)在室温下自发进行,则该反应的△H<0 | |
| D. | 向浓度均为0.1mol•L-1KI和NaCl混合溶液中,滴加几滴硝酸镍溶液,只得到AgI沉淀说明Ksp(Agl)<Ksp(AgCl) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ;
;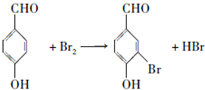 ;
; .a.属于酯类 b.能发生银镜反应 c.与FeCl3溶液发生显色反应①
.a.属于酯类 b.能发生银镜反应 c.与FeCl3溶液发生显色反应①查看答案和解析>>
科目:高中化学 来源: 题型:解答题
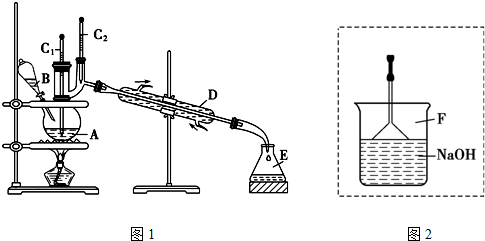
| 苯 | 溴 | 溴苯 | |
| 密度/g•cm-3 | 0.88 | 3.10 | 1.50 |
| 沸点/℃ | 80 | 59 | 156 |
| 水中溶解度 | 微溶 | 微溶 | 微溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属钠浮在水面上 | B. | 金属钠形成小球状 | ||
| C. | 金属钠在水面上迅速游动 | D. | 反应后的溶液呈现红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 四氯化碳分子的比例模型: | B. | 如图所示一定代表丙烯 | ||
| C. | 12C32S2比12C34S2更易挥发 | D. | O${\;}_{2}^{2-}$电子式为: |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5.6 | B. | 1.6 | C. | 3.2 | D. | 3.6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com