
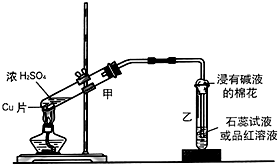
 实验室常用下列装置来进行铜跟浓硫酸反应等一系列实验.
实验室常用下列装置来进行铜跟浓硫酸反应等一系列实验.分析 (1)二氧化硫检验漂白性,通常用品红溶液检验二氧化硫;铜与浓硫酸在加热条件下反应生成硫酸铜、二氧化硫和水;
(2)硫酸铜与水显示蓝色;
(3)二氧化硫有毒的酸性气体,所以饱和碳酸钠溶液是防止二氧化硫污染;
(4)二氧化硫具有漂白性,能够使品红溶液褪色;二氧化硫的漂白是生成了一种不稳定的无色物质,为暂时的,加热后会恢复;
(5)木炭跟浓硫酸反应生成二氧化硫、二氧化碳和水.
解答 解:(1)浓硫酸和铜在加热的条件下生成硫酸铜、二氧化硫和水,由于二氧化硫具有漂白性,能使得品红溶液褪色,故常用品红溶液验证二氧化硫的存在,即品红褪色,则证明有二氧化硫生成;铜跟浓硫酸反应,铜具有还原性,浓硫酸具有强氧化性,反应必须加热才能发生,书写化学方程式时注意“浓”字,反应的化学方程式为:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O,
故答案为:乙中品红溶液褪色;Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O;
(2)待试管中的液体冷却后,将试管上层液体倒去,再慢慢加入少量水,可观察溶液呈蓝色,故答案为:蓝;
(3)装置乙的试管口部放有一团浸有碱液的棉花,棉花中通常是浸有饱和碳酸钠溶液,其作用是:除去尾气SO2,防污染,故答案为:除去尾气SO2,防污染;
(4)二氧化硫能够使品红溶液褪色,所以生成的气体使品红溶液的颜色褪色;
二氧化硫的漂白原理为:二氧化硫与有色物质生成了一种不稳定的无色物质,加热后生成的无色物质分解,又恢复原来的颜色,所以取少量乙试管中溶液于试管中加热,溶液会由无色变成红色,
故答案为:由无色变红色;二氧化硫漂白时生成不稳定的无色物质;
(5)木炭跟浓硫酸反应生成二氧化硫、二氧化碳和水,反应的化学方程式为:C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2+2SO2+2H2O,故答案为:C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2+2SO2+2H2O.
点评 本题考查了铜与浓硫酸的性质,题目难度中等,试题涉及铜与浓硫酸的反应、二氧化硫的性质及检验、性质实验方案的设计与评价等知识,注意明确二氧化硫与氯水的漂白原理的区别.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 含有NA个氦原子的氦气在标准状况下的体积约为22.4L | |
| B. | 常温常压下,28g N2中含有的原子数为NA | |
| C. | 标准状况下22.4L Cl2与足量的水充分反应,转移的电子数为NA | |
| D. | 标准状况下,11.2LH2O含有的分子数为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 莫言 | B. | 屠呦呦 | C. | 侯德榜 | D. | 徐光宪 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子化合物中一定含有离子键 | |
| B. | 单质的分子中均不存在化学键 | |
| C. | 含有共价键的化合物一定是共价化合物 | |
| D. | 任何物质内都含有化学键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 自然界存在大量单质硅 | B. | 光导纤维被广泛应用于信息传输 | ||
| C. | SiO2与任何酸都不起反应 | D. | 盛NaOH溶液的试剂瓶塞可用玻璃塞 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com