
| A. | H2O、CO2 | B. | MgF2、H2O2 | C. | NaOH、Ba(OH)2 | D. | NaCl、KCl |
分析 一般来说,活泼金属和活泼非金属元素之间易形成离子键,不同非金属元素之间易形成极性共价键,同种非金属元素之间易形成极性共价键,第IA族(H元素除外)、第IIA族和第VIA族、第VIIA族元素之间易形成离子键,以此解答该题.
解答 解:A.水分子和二氧化碳分子中都只含极性共价键,所以化学键类型相同,故A错误;
B.氟化镁中只含离子键,H2O2含共价键,所以化学键类型有差异,故B正确;
C.氢氧化钠和氢氧化钡中都含有离子键和共价键,所以化学键类型相同,故C错误;
D.氯化钠和氯化钾中都只含离子键,所以化学键类型相同,故D错误;
故选B.
点评 本题考查了化学键的判断,为高频考点,知道离子键和共价键的区别,注意氟化镁中两个氟离子之间不存在化学键,为易错点.


 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案科目:高中化学 来源: 题型:解答题
 尿素是蛋白质代谢的产物,也是重要的化学肥料,工业合成尿素反应如下:2NH3(g)+CO2(g)?CO(NH2)2(s)+H2O(g)
尿素是蛋白质代谢的产物,也是重要的化学肥料,工业合成尿素反应如下:2NH3(g)+CO2(g)?CO(NH2)2(s)+H2O(g)| 温度(℃) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡气体总浓度(10-3mol/L) | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 温度 | 时间/min n/mol | 0 | 10 | 20 | 40 | 50 |
| T1 | n(CH4) | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
| T2 | n(CH4) | 0.50 | 0.30 | 0.18 | … | 0.15 |
| A. | 10min内,T1时CH4的化学反应速率比T2时小 | |
| B. | T1<T2 | |
| C. | 平衡常数:K(T1)<K(T2) | |
| D. | a<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
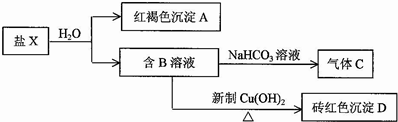
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A原子的最外层电子数比B原子的最外层电子数少 | |
| B. | A原子的电子层数比B原子的电子层数多 | |
| C. | 1mol A从酸中置换H+生成的H2比1mol B从酸中置换H+生成的H2多 | |
| D. | 常温时,A能从水中置换出氢,而B不能 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
 .
.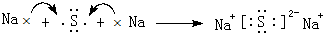 ,该化合物属于离子(填“共价”或“离子”)化合物.
,该化合物属于离子(填“共价”或“离子”)化合物. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH2COOH | B. | HCOOCH2CH3 | C. | CH3COOCH3 | D. | CH3COCH2OH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯和浓溴水用Fe作为催化剂制溴苯 | |
| B. | 氯乙烷与NaOH溶液共热,在水解后的溶液中加入AgNO3溶液检验Cl- | |
| C. | CH4与Cl2在光照条件下得到纯净的CH3Cl | |
| D. | 乙烯通入溶有Br2的CCl4溶液可得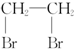 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com