
某元素原子的质量数为52,中子数为28,其基态原子未成对电子数为()
A. 1 B. 3 C. 4 D. 6
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
在硫酸铝、硫酸钾和明矾的混合溶液中,SO42﹣的浓度为0.4mol/L,当加入等体积0.4mol/L KOH溶液时,生成的沉淀恰好完全溶解.则反应后溶液中K+的浓度约为( )
|
| A. | 0.225mol/L | B. | 0.25mol/L | C. | 0.45mol/L | D. | 0.9mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
某有机物甲经氧化得到乙(分子式为C2H3O2Cl);而甲经水解可得丙,1mol丙和2mol乙反应得一种含氯的酯(C6H8O4Cl2);由此推断甲的结构简式为( )
|
| A. | ClCH2CH2OH | B. | OHC﹣O﹣CH2Cl | C. | ClCH2CHO | D. | HOCH2CH2OH |
查看答案和解析>>
科目:高中化学 来源: 题型:
a mol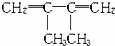 和b mol CH2=CH﹣CN按一定比例加聚成高分子化合物A.一定量的A完全燃烧生成CO2(g)、H2O(g)和N2(g),其中CO2的体积分数为57.14%,则形成A的两有机物的物质的量比为( )
和b mol CH2=CH﹣CN按一定比例加聚成高分子化合物A.一定量的A完全燃烧生成CO2(g)、H2O(g)和N2(g),其中CO2的体积分数为57.14%,则形成A的两有机物的物质的量比为( )
|
| A. | 1:1 | B. | 1:2 | C. | 2:3 | D. | 3:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某元素X的气态氢化物在高温下分解为固态的X单质和H2,分解反应前后气体的质量之比是17:1.下列有关叙述中错误的是()
A. X的阴离子的电子排布式是1s22s22p63s23p6
B. X的最高价氧化物对应的水化物的酸性比砷酸强
C. X的最高价氧化物中,X的质量分数为50%
D. X的气态氢化物的水溶液呈酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)以下列出的是一些原子的2p能级和3d能级中电子排布的情况.试判断,哪些违反了泡利原理③,哪些违反了洪特规则④.
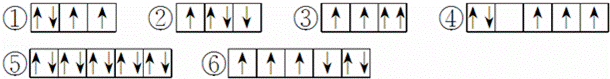
(2)某元素的激发态(不稳定状态)原子的电子排布式为 ,则该元素基态原子的电子排布式为 ;其最高价氧化物对应水化物的化学式是 .
(3)将下列多电子原子的原子轨道按轨道能量由低到高顺序排列 .
①2s②3d③4s④3s⑤4p⑥3p.
查看答案和解析>>
科目:高中化学 来源: 题型:
下列电离方程式中,正确的是()
A. Na2SO4=2Na++SO4﹣2 B. Ba(OH)2=Ba2++OH2﹣
C. Ca(NO3)2=Ca2++2(NO3)2﹣ D. Al2(SO4)3=2Al3++3SO42﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
海水中含量较高的金属元素有Na、Mg、Ca等,地壳中含量最高的Al、Fe在海水中的含量却极低,以至食盐提纯过程一般无需考虑除Fe3+、Al3+或AlO2﹣.为什么海水中Al元素的含量极低? .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com