
在t℃时,将agNH3完全溶解于水,得到Vml溶液,假设该溶液的密度为ρg/cm3,质量分数为w,其中含NH4+的物质的量为bmol。下列叙述中不正确的是
A.溶质的质量分数w=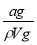 ×100%
×100%
B.溶质的物质的量浓度c=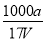 mol/L
mol/L
C.溶液中c(OH-)= 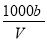 mol/L+c(H+)
mol/L+c(H+)
D.上述溶液中再加入Vml水后,所得溶液的质量分数大于0.5w
 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源:2016-2017学年辽宁省高二上10月月考化学试卷(解析版) 题型:实验题
用已知浓度的HCl溶液测定未知浓度的氨水,选用的指示剂_____________
(2)取体积相同的、物质的量浓度相同的两分NaOH溶液,把其中的一份放空气中一段时间后。用已知浓度的硫酸中和上述这两份溶液,若中和第一份(放在空气中一段时间)所消耗硫酸溶液体积为V1,另一份消耗硫酸溶液体积为V2,
①若以甲基橙为指示剂时,V1和V2的关系是_ ___
②若以酚酞为指示剂时,V1和V2的关系是__ ____
(3)用酸式滴定管准确移取25.00mL某未知浓度的盐酸于一洁净的锥形瓶中,然后用 0.20mol·L-1的氢氧化钠溶液(指示剂为酚酞).滴定结果如下:
| NaOH起始读数 | NaOH终点读数 |
第一次 | 0.10mL | 18.60mL |
第二次 | 0.30mL | 18.00mL |
①根据以上数据可以计算出盐酸的物质的量浓度为 mol·L-1.
②达到滴定终点的标志是_______________
③以下操作造成测定结果偏高的原因可能是 。
A. 配制标准溶液的氢氧化钠中混有Na2CO3杂质
B. 滴定终点读数时,俯视滴定管的刻度,其它操作均正确
C. 盛装未知液的锥形瓶用蒸馏水洗过,未用待测液润洗
D. 滴定到终点读数时发现滴定管尖嘴处悬挂一滴溶液
E. 未用标准液润洗碱式滴定管
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高二上第一次月考化学试卷(解析版) 题型:选择题
N2(g)与H2(g)在铁催化剂表面经历如右过程生成NH3(g):
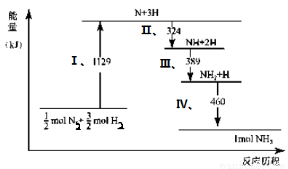
下列说法正确的是( )
A.Ⅰ中1129KJ为该反应过程的活化能
B.N2(g)+3H2(g) 2NH3(g) ΔH=2(324+389+460-1129)kJ/mol
2NH3(g) ΔH=2(324+389+460-1129)kJ/mol
C.Ⅱ、Ⅲ、Ⅳ均为放热过程
D.N2(g)+3H2(g) 2NH3(g)ΔH>0
2NH3(g)ΔH>0
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上学期第二次月考化学试卷(解析版) 题型:选择题
下表中对应关系错误的是( )
A | NaCl===Na++Cl-; NH3·H2O | 均属于电离方程式 |
B | Ba2++SO42- ===BaSO4↓; HCO3-+OH-===CO32- +H2O | 均可表示一类反应 |
C | SO2使酸性高锰酸钾溶液褪色;SO2使碱性酚酞溶液褪色 | 均利用SO2的同一性质 |
D | Cl2+2NaOH===NaCl+NaClO+H2O; 3S+6NaOH===2Na2S+Na2SO3+3H2O | Cl2和S在反应中既作氧化剂又作还原剂 |
查看答案和解析>>
科目:高中化学 来源:2017届安徽省高三上学期第二次月考化学试卷(解析版) 题型:实验题
一种含铝、锂、钴的新型电子材料,生产中产生的废料数量可观,废料中的铝以金属铝箔的形式;钴以Co2O3·CoO的形式存在,吸附在铝箔的单面或双面;锂混杂于其中,从废料中回收氧化钴(CoO)的工艺流程如下:

(1)过程I中采用NaOH溶液溶出废料中的Al,能加快溶出率的操作有 、 。(写出两条)
(2)过程II中加入稀H2SO4酸化后,再加入Na2S2O3溶液浸出钴,则浸出钴的离子反应方程式为 (产物中只有一种酸根)。请从反应原理分析不用盐酸浸出钴的主要原因 。
(3)碳酸钠溶液在过程III和IV中所起作用有所不同,请分别用离子方程式表示在过程III、IV中起的作用: ; 。
查看答案和解析>>
科目:高中化学 来源:2017届安徽省高三上学期第二次月考化学试卷(解析版) 题型:选择题
锑(Sb)在自然界一般以硫化物的形式存在。从硫化物中提取单质锑一般是先在高温下将硫化物转化为氧化物,再用碳还原①2Sb2S3+3O2+6Fe=Sb4O6+6FeS ②Sb4O6+6C=4Sb+6CO,下列关于反应①、②的说法正确的是
A.反应①②中的氧化剂分别是Sb2S3、Sb4O6
B.反应①中每生成3molFeS时,共转移6mol电子
C.反应②说明高温下Sb的还原性比C强
D.每生成4molSb时,反应①与反应②中还原剂的物质的量之比为3:1
查看答案和解析>>
科目:高中化学 来源:2017届安徽省高三上学期第二次月考化学试卷(解析版) 题型:选择题
NA代表阿伏伽德罗常数的值,下列说法正确的是
A.0.1molCl2溶于足量水中,转移的电子数为0.1NA
B.100g98%的浓硫酸中,氧原子总数为4NA
C.常温常压下,3g甲醛所含σ键数目为0.3NA
D.1molFeCl3与沸水反应生成胶体后,含有的Fe(OH)3胶粒数目为NA
查看答案和解析>>
科目:高中化学 来源:2016-2017学年宁夏高一上第一次月考化学试卷(解析版) 题型:选择题
下列实验操作中错误的是
A. 蒸发操作时,应使混合物中出现大量固体后,停止加热
B. 蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处
C. 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
D. 萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
查看答案和解析>>
科目:高中化学 来源:2016-2017学年陕西省高二上10月月考化学试卷(解析版) 题型:选择题
某温度下,浓度都是1 mol·L-1的两种气体X2和Y2,在密闭容器中发生反应生成气体Z,反应2 min后,测得参加反应的X2的浓度为0.6 mol·L-1,用Y2的浓度变化表示的化学反应速率v(Y2)=0.1 mol·L-1·min-1,生成的c(Z)为0.4 mol/L。则该反应的化学方程式是
A.X2+2Y2=2Z B.2X2+Y2=2Z
C.3X2+Y2=2Z D.X2+3Y2=2Z
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com