
| ��� | �� | �� | �� | �� | �� | �� |
| ������װ��ͼ |  |  |  |  |  |  |
���� ��Ũ������������̷��������������Ӻ���ͭ��Ӧ�����Ȼ�ͭ��β���������������գ�������������˳��Ϊ���ۢݢڢܢ٢ޣ���Ӧ���ɵ������л���HCl������б���ʳ��ˮ�ɳ��ӣ��ڢ��з���Cu+Cl2$\frac{\underline{\;\;��\;\;}}{\;}$CuCl2������������β��������Cl2+2NaOH=NaCl+NaClO+H2O��ʵ����ע�������ų�װ���еĿ������Դ������
��� �⣺��ȡ��������ˮ�Ȼ�ͭ����������˳��Ϊ���ۢݢڢܢ٢ޣ�
��1�����ڢ����ʱ������м���Һ��������DZ���ʳ��ˮ���ɳ�ȥHCl���ʴ�Ϊ������ʳ��ˮ��
��2��װ�â�Ϊ�Ʊ�������������Ӧ�Ļ�ѧ����ʽ��MnO2+4HCl$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+2Cl2��+2H2O���ʴ�Ϊ��MnO2+4HCl$\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+2Cl2��+2H2O��
��3���Ʊ��Ȼ�ͭʱ��Ӧ���ų�װ���еĿ��������ȵ�ȼ�ݴ��ľƾ��ƣ�����CuCl2�к���CuO���ʣ�����ַ�Ӧ��װ�âٵIJ������ʣ����CuCl2���ػ�ɫ��
�ʴ�Ϊ���ݣ�CuO���ػƣ�
��4���ڢٺ͢�֮��������һ��ʢ��Ũ�����ϴ��ƿ���������Ƿ�ֹ����������Һ�е�ˮ��������װ�â٣��ʴ�Ϊ����ֹ����������Һ�е�ˮ��������װ�â٣�
���� ���⿼�����ʵ��Ʊ�ʵ�飬Ϊ��Ƶ���㣬�����������Ʊ����Ȼ�ͭ���Ʊ���Ӧ��ʵ��װ�õ�����Ϊ���Ĺؼ������ط�����ʵ�������Ŀ��飬��Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 10s�ڣ�NH3��ƽ����Ӧ����Ϊ0.008mol•L-1•s-1 | |
| B�� | �÷�Ӧ�ﵽƽ��ʱ6v��O2����=5v��H2O���� | |
| C�� | 10s�ڣ���Ӧ�ų�������Ϊ0.1akJ | |
| D�� | 10sʱ��H2O�ķ�Ӧ����Ϊ0.012mol•L-1•s-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������һ�����ʵ���Ũ����Һ��ʵ����������ƽ���������DZ������� | |
| B�� | ʵ�����У�ʢװNaOH�ȼ�����Һ���Լ�ƿ����Ƥ�� | |
| C�� | ����ϡNaOH��Һ��û�в���ʹʪ��ĺ�ɫʯ����ֽ���������壬���δ֪Һ�в���NH4+ | |
| D�� | ��pH��ֽ�ⶨij��Һ��pHʱ����Ԥ��������ˮʪ��pH��ֽ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
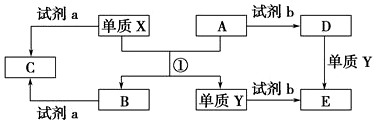
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | v��A��=v��B�� | B�� | v��A��=2v��C�� | C�� | 2v��B��=3v��C�� | D�� | 3v��B��=v��D�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ԫ�ص縺��Խ���ԭ�ӣ��������ӵ�����Խǿ | |
| B�� | ��NH4+ ��[Cu��NH3��4]2+�ж�������λ�� | |
| C�� | SO2��SO3���Ǽ��Է��� | |
| D�� | NF3��NH3������Cu2+���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

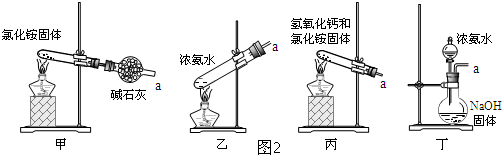
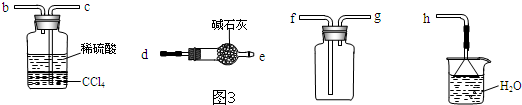
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com