
多晶硅是太阳能光伏产业的重要原材料。
(1)由石英砂可制取粗硅,反应式为SiO2(s)+2C(s)===Si(s)+2CO(g),粗硅提纯常见方法之一是先将粗硅与HCl制得SiHCl3,经提纯后再用H2还原:
SiHCl3(g)+H2(g) Si(s)+3HCl(g)。
Si(s)+3HCl(g)。
不同温度及不同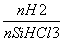 时,反应物X的平衡转化率关系如图所示。
时,反应物X的平衡转化率关系如图所示。
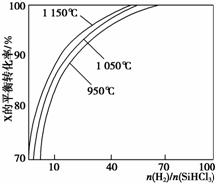
①X是 ▲ (填“H2”或“SiHCl3”)。
 ②上述反应的平衡常数K(1150 ℃) ▲ K(950 ℃)(填“>”、“<”或“=”)。
②上述反应的平衡常数K(1150 ℃) ▲ K(950 ℃)(填“>”、“<”或“=”)。
(2)SiH4(硅烷)法生产高纯多晶硅是非常优异的方法。
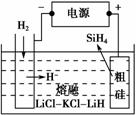
①用粗硅作原料,熔融盐电解法制取硅烷原理如图所示,电解时阳极的电极反应式为 ▲ 。
②硅基太阳电池需用N、Si两种元素组成的化合物Y作钝化材料,它可由SiH4与NH3混合气体进行气相沉积得到,已知Y中Si的质量分数为60%,Y的化学式为 ▲ 。
 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案科目:高中化学 来源: 题型:
氢氧燃料电池已用于航天飞机。以30%KOH溶液为电解质溶液的这种电池在使用时的电极反应如下:2H2 + 4OH- - 4e- = 4H2O;O2 + 2H2O + 4e- = 4OH-。据此作出判断,下列说法中错误的是:
A.H2在负极发生氧化反应
B.供电时的总反应为:2H2+O2=2H2O
C.产物为无污染的水,属于环境友好电池
D.燃料电池的能量转化率可达100%
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,某恒定容积的密闭容器中发生如下可逆反应:CO(g)+H2(g)  C(s)+H2O(g);ΔH>0,以1 mol CO和2 mol H2为起始反应物,t1时达到平衡,生成0.5mol H2O(g)。t2时改变反应条件,化学反应速率(v)与时间(t)的关系如图所示。下列叙述正确的是
C(s)+H2O(g);ΔH>0,以1 mol CO和2 mol H2为起始反应物,t1时达到平衡,生成0.5mol H2O(g)。t2时改变反应条件,化学反应速率(v)与时间(t)的关系如图所示。下列叙述正确的是
A.t2时改变的条件可能是升高了温度或增大了压强
B.平衡后若加入少量炭,平衡向逆反应方向移动
C.平衡后若加入氢气,上述反应的ΔH会增大
D.起始时刻和达平衡后容器的压强之比为5∶6

查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是
A.在原电池的负极和电解池的阴极上都发生失电子的氧化反应
B.用惰性电极电解Na2SO4溶液,阴阳两极产物的物质的量之比为1∶2
C.用惰性电极电解饱和NaCl溶液,若有1 mol电子转移,则生成1 mol NaOH
D.镀层破损后,镀锡铁板比镀锌铁板更耐腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
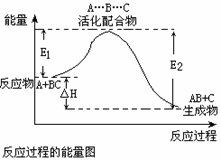
某反应过程中体系的能量变化如图所示,下列说法错误的是
A.反应过程可表示为A+BC—→[A…B…C] —→AB+C
(反应物) (过渡态) (产物)
B.E1为反应物的平均能量与过渡态的能量差,称为正反应的活化能
C.正反应的热效应为△H=E1—E2,且E2>E1,所以正反应为放热反应
D.此图中逆反应的热效应△H=E1—E2,为吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、M、N是短周期主族元素,且原子序数依次增大。已知X的最外层电子数是电子层数的3倍,X、M同主族,Y的原子在短周期主族元素中原子半径最大。下列说法正确的是
A.M与X形成的化合物对应的水化物一定是强酸
B.Y2X和Y2X2中化学键类型完全相同
C.X、Y的简单离子半径:r(X2-)>r(Y+)
D.M的气态氢化物比N的气态氢化物稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的值,下列叙述错误的是 ( )。
A.18 g H2O中含有的质子数为10NA
B.12 g金刚石中含有的共价键数为4NA
C.46 g NO2和N2O4混合气体中含有原子总数为3NA
D.1 mol Na与足量O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电
子
查看答案和解析>>
科目:高中化学 来源: 题型:
钼是一种过渡金属元素,通常用作合金及不锈钢的添加剂,这种元素可增强合金的强度、硬度、可焊性及韧性,还可增强其耐高温及耐腐蚀性能。如图是化工生产中制备金属钼的主要流程图。
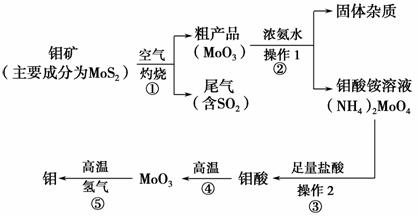
(1)写出反应①的化学方程式:________________________________________。
(2)反应①的尾气可以再利用,写出应用该尾气制得的两种重要化学试剂________________________________________________________________。
(3)如果在实验室模拟操作1和操作2,则需要使用的主要玻璃仪器有_________________________________________________________________。
(4)钼在空气中灼烧生成三氧化钼,三氧化钼溶于氢氧化钠溶液生成钼酸钠;三氧化钼不溶于盐酸或稀硫酸。钼酸钠的化学式为________。
(5)工业上制备还原性气体CO和H2的反应原理为CO2+CH4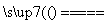 2CO+2H2,CH4+H2O
2CO+2H2,CH4+H2O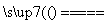 CO+3H2。含甲烷体积分数为80%的a L(标准状况)天然气与足量二氧化碳和水蒸气的混合物在高温下反应,甲烷转化率为90%,用产生的还原性气体(CO和H2)还原MoO3制钼,理论上能生产钼的质量为________。
CO+3H2。含甲烷体积分数为80%的a L(标准状况)天然气与足量二氧化碳和水蒸气的混合物在高温下反应,甲烷转化率为90%,用产生的还原性气体(CO和H2)还原MoO3制钼,理论上能生产钼的质量为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com