
I��ijУ��ѧʵ��С��̽��Ũ�ȶԻ�ѧ��Ӧ���ʵ�Ӱ�죬���ⶨ![]() ��KI��Ӧ�Ļ�ѧ��Ӧ���ʡ���������ʵ��̽����
��KI��Ӧ�Ļ�ѧ��Ӧ���ʡ���������ʵ��̽����
��ʵ��ԭ����
![]() ��KI��Ӧ�����ӷ���ʽΪ��
��KI��Ӧ�����ӷ���ʽΪ��
![]() (1)
(1)
ƽ����Ӧ���ʵļ���ʽΪ![]() ��
��
ʵ��ʱ����![]() ��
��![]() �͵���ָʾ�������Һ�м���
�͵���ָʾ�������Һ�м���![]() ��Һ�����Ͻ��衣
��Һ�����Ͻ��衣
�ڷ�Ӧ(1)���е�ͬʱ��������Ӧ��
![]() (2)
(2)
��Ӧ(1)���ɵ�![]() ������
������![]() ��Ӧ��������ɫ��
��Ӧ��������ɫ��![]() ��
��![]() ��
��![]() �ľ�ʱ����Ӧ(1)�������ɵ�
�ľ�ʱ����Ӧ(1)�������ɵ�![]() ����������ó�����ɫ���Ӽ���
����������ó�����ɫ���Ӽ���![]() ��Һ��������ɫ��ʱ��Ϊ
��Һ��������ɫ��ʱ��Ϊ![]() ��
��
��ʵ�����ݡ�
��1��ʵ��С����Ƶ�ʵ���¼�������ݼ�¼���£��뽫������ĸ��ʾ�Ŀո����ϡ�
| ʵ���� | �� | �� | �� | �� | �� | |
| �Լ� ���� ��mL�� | 0.20 mol��L | 20.0 | 10.0 | b | 20.0 | 20.0 |
| 0.20 mol��L | 20.0 | 20.0 | 20.0 | 10.0 | 5.0 | |
| 0.010 mol��L | a | 8.0 | 8.0 | 8.0 | 8.0 | |
| 0.2%������Һ | 2.0 | 2.0 | 2.0 | 2.0 | 2.0 | |
| 0.20 mol��L | 0 | 0 | 0 | 10.0 | c | |
| 0.20 mol��L | 0 | 10.0 | 15.0 | 0 | 0 | |
| 20��ʱ����Ӧʱ�� | 32 | 67 | 130 | 66 | 135 | |
| Ϊ��ʹ��Һ������ǿ�Ⱥ���������ֲ��䣬���ٵ�(NH4)2S2O8��Һ��KI��Һ���������ֱ���(NH4)2SO4��Һ��KNO3��Һ���㣻��Һ��Ϻ�������� | ||||||
��2��Ϊ��ʹ��Ӧ��ֽ��У�����������ʵ�������Ӧ�ò��Ͻ��еIJ����� ��
��3���ڢ���ʵ���![]() mol��(L��s)
mol��(L��s)![]() ��
��
��4�������ϱ����ݷ��������Եõ��Ľ�����(д��һ������) ��
II��ʵ��С������ϵ�֪������NaCO3��Na2S��Һ��ͨ��SO2�������Ʊ�����ʵ�������Na2S2O3����Ӧ���£�
![]()
![]()
![]()
��С���������ԭ�������ͼ19��ʾװ���Ʊ�![]() ��
��

��1��ʵ��Ӧ�����к������ŷŵ������С�װ�â١�����ʢ�ŵ��Լ������Ǣ� ���� ��
��2��ʵ������У����������ͨ�룬װ�â����д�����ɫ��������������ͨ�����壬���Թ۲쵽�������� ��
��3����Ӧ�������Ƶõ�![]() ϡ��Һ�еõ�
ϡ��Һ�еõ�![]() �������Ҫ���������� ��
�������Ҫ���������� ��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
I��ijУ��ѧʵ��С��̽��Ũ�ȶԻ�ѧ��Ӧ���ʵ�Ӱ�죬���ⶨ![]() ��KI��Ӧ�Ļ�ѧ��Ӧ���ʡ���������ʵ��̽����
��KI��Ӧ�Ļ�ѧ��Ӧ���ʡ���������ʵ��̽����
��ʵ��ԭ����
![]() ��KI��Ӧ�����ӷ���ʽΪ��
��KI��Ӧ�����ӷ���ʽΪ��
![]() ��1��
��1��
ƽ����Ӧ���ʵļ���ʽΪ![]() ��
��
ʵ��ʱ����![]() ��
��![]() �͵���ָʾ�������Һ�м���
�͵���ָʾ�������Һ�м���![]() ��Һ�����Ͻ��衣�ڷ�Ӧ��1�����е�ͬʱ��������Ӧ��
��Һ�����Ͻ��衣�ڷ�Ӧ��1�����е�ͬʱ��������Ӧ��
![]() ��2��
��2��
��Ӧ��1�����ɵ�![]() ������
������![]() ��Ӧ��������ɫ��
��Ӧ��������ɫ��![]() ��
��![]() ��
��![]() �ľ�ʱ����Ӧ��1���������ɵ�
�ľ�ʱ����Ӧ��1���������ɵ�![]() ����������ó�����ɫ���Ӽ���
����������ó�����ɫ���Ӽ���![]() ��Һ��������ɫ��ʱ��Ϊ
��Һ��������ɫ��ʱ��Ϊ![]() ��
��
��ʵ�����ݡ�
��1��ʵ��С����Ƶ�ʵ���¼�������ݼ�¼���£��뽫������ĸ��ʾ�Ŀո����ϡ�
| ʵ���� | ��[��Դ:Z��xx��k.Com] | �� | �� | �� | �� | |
| �Լ�[��Դ:ѧ&��&��Z&X&X ���� ��mL�� | 0��20 mol��L | 20��0 | 10��0[ | b | 20��0 | 20��0 |
| 0��20 mol��L | 20��0 | 20��0 | 20��0 | 10��0 | 5��0 | |
| 0��010 mol��L | a | 8��0 | 8��0 | 8��0 | 8��0 | |
| 0��2%������Һ | 2��0 | 2��0 | 2��0 | 2��0 | 2��0 | |
| 0��20 mol��L | 0 | 0 | 0 | 10��0 | c | |
| 0��20 mol��L | 0 | 10��0 | 15��0 | 0 | 0 | |
| 20��ʱ����Ӧʱ�� | 32 | 67 | 130 | 66 | 135 | |
| Ϊ��ʹ��Һ������ǿ�Ⱥ���������ֲ��䣬���ٵģ�NH4��2S2O8��Һ��KI��Һ���������ֱ��ã�NH4��2SO4��Һ��KNO3��Һ���㣻��Һ��Ϻ�������� | ||||||
��2��Ϊ��ʹ��Ӧ��ֽ��У�����������ʵ�������Ӧ�ò��Ͻ��еIJ����� ��
��3���ڢ���ʵ���![]() mol����L��s��
mol����L��s��![]() ��
��
��4�������ϱ����ݷ��������Եõ��Ľ����У�д��һ�����ɣ� ��
II��ʵ��С������ϵ�֪������NaCO3��Na2S��Һ��ͨ��SO2�������Ʊ�����ʵ�������Na2S2O3����Ӧ���£�
![]()
![]()
![]()
��С���������ԭ�������ͼ19��ʾװ���Ʊ�![]() ��
��

��1��ʵ��Ӧ�����к������ŷŵ������С�װ�â١�����ʢ�ŵ��Լ������Ǣ� ��
�� ��
��2��ʵ������У����������ͨ�룬װ�â����д�����ɫ��������������ͨ�����壬���Թ۲쵽�������� ��
��3����Ӧ�������Ƶõ�![]() ϡ��Һ�еõ�
ϡ��Һ�еõ�![]() �������Ҫ���������� ��
�������Ҫ���������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
��13�֣�I��ijУ��ѧʵ��С��̽��Ũ�ȶԻ�ѧ��Ӧ���ʵ�Ӱ�죬���ⶨ(NH4)2S2O8��KI��Ӧ�Ļ�ѧ��Ӧ���ʡ���������ʵ��̽����
��ʵ��ԭ����
(NH4)2S2O8��KI��Ӧ�����ӷ���ʽΪ��S2O82�� + 2I��= 2SO42�� + I2 ��1��
ƽ����Ӧ���ʵļ���ʽΪv(S2O82��)= ��
ʵ��ʱ����KI��Na2S2O3�͵���ָʾ�������Һ�м���(NH4)2S2O8��Һ�����Ͻ��衣
�ڷ�Ӧ��1�����е�ͬʱ��������Ӧ��2S2O32��+ I2 = S4O62��+ 2I�� ��2��
��Ӧ(1)���ɵ�I2������S2O32����Ӧ��������ɫ��S4O62����I����S2O32���ľ�ʱ����Ӧ��1���������ɵ�I2����������ó�����ɫ���Ӽ���(NH4)2S2O8��Һ��������ɫ��ʱ��Ϊ��t��
��ʵ�����ݡ�
��1��ʵ��С����Ƶ�ʵ���¼�������ݼ�¼���£��뽫������ĸ��ʾ�Ŀո����ϡ�
| ʵ �� �� �� | �� | �� | �� | �� | �� | |
|
�Լ� ���� (mL) | 0.20 mol��L-1 (NH4)2S2O8��Һ | 20.0 | 10.0 | b | 20.0 | 20.0 |
| 0.20 mol��L-1 KI��Һ | 20.0 | 20.0 | 20.0 | 10.0 | 5.0 | |
| 0.010 mol��L-1 Na2S2O3��Һ | a | 8.0 | 8.0 | 8.0 | 8.0 | |
| 0.2% ������Һ | 2.0 | 2.0 | 2.0 | 2.0 | 2.0 | |
| 0.20 mol��L-1KNO3��Һ | 0 | 0 | 0 | 10.0 | c | |
| 0.20 mol��L-1(NH4)2SO4��Һ | 0 | 10.0 | 15.0 | 0 | 0 | |
| 20 ��ʱ����Ӧʱ�䦤t��s�� | 32 | 67 | 130 | 66 | 135 | |
| Ϊ��ʹ��Һ������ǿ�Ⱥ���������ֲ��䣬���ٵ�(NH4)2S2O8��Һ��KI��Һ���������ֱ���(NH4)2SO4��Һ��KNO3��Һ���㣻��Һ��Ϻ�������� |
��2��Ϊ��ʹ��Ӧ��ֽ��У�����������ʵ�������Ӧ�ò��Ͻ��еIJ����� ��
��3���ڢ���ʵ���v(S2O82��)= mol��(L��s)-1��
��4�������ϱ����ݷ��������Եõ��Ľ����У�д��һ�����ɣ�
��
II��ʵ��С������ϵ�֪������Na2CO3��Na2S��Һ��ͨ��SO2�������Ʊ�����ʵ�������Na2S2O3����Ӧ���£�Na2CO3+ SO2= Na2SO3 + CO2��2Na2S + 3SO2= 2Na2SO3 + 3S����
Na2SO3 + S= Na2S2O3����С���������ԭ�������ͼ��ʾװ���Ʊ�Na2S2O3��
��1��ʵ��Ӧ�����к������ŷŵ������С�װ�â١�����ʢ�ŵ��Լ�������
�� ��
�� ��
��2��ʵ������У����������ͨ�룬װ�â��������ݲ��������д�����ɫ��������������ͨ�����壬���Թ۲쵽�������� ��
��3����Ӧ�������Ƶõ�Na2S2O3ϡ��Һ�еõ�Na2S2O3��5H2O�������Ҫ���������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010-2011������ʡ�߶���ѧ����ĩ���Ի�ѧ�Ծ� ���ͣ�ʵ����
��13�֣�I��ijУ��ѧʵ��С��̽��Ũ�ȶԻ�ѧ��Ӧ���ʵ�Ӱ�죬���ⶨ(NH4)2S2O8��KI��Ӧ�Ļ�ѧ��Ӧ���ʡ���������ʵ��̽����
��ʵ��ԭ����
(NH4)2S2O8��KI��Ӧ�����ӷ���ʽΪ��S2O82�� + 2I��= 2SO42�� + I2 ��1��
ƽ����Ӧ���ʵļ���ʽΪv(S2O82��)=  ��
��
ʵ��ʱ����KI��Na2S2O3�͵���ָʾ�������Һ�м���(NH4)2S2O8��Һ�����Ͻ��衣
�ڷ�Ӧ��1�����е�ͬʱ��������Ӧ��2S2O32��+ I2 = S4O62��+ 2I�� ��2��
��Ӧ(1)���ɵ�I2������S2O32����Ӧ��������ɫ��S4O62����I����S2O32���ľ�ʱ����Ӧ��1���������ɵ�I2����������ó�����ɫ���Ӽ���(NH4)2S2O8��Һ��������ɫ��ʱ��Ϊ��t��
��ʵ�����ݡ�
��1��ʵ��С����Ƶ�ʵ���¼�������ݼ�¼���£��뽫������ĸ��ʾ�Ŀո����ϡ�
|
ʵ �� �� �� |
�� |
�� |
�� |
�� |
�� |
|
|
�Լ� ���� (mL) |
0.20 mol��L-1 (NH4)2S2O8��Һ |
20.0 |
10.0 |
b |
20.0 |
20.0 |
|
0.20 mol��L-1 KI��Һ |
20.0 |
20.0 |
20.0 |
10.0 |
5.0 |
|
|
0.010 mol��L-1 Na2S2O3��Һ |
a |
8.0 |
8.0 |
8.0 |
8.0 |
|
|
0.2% ������Һ |
2.0 |
2.0 |
2.0 |
2.0 |
2.0 |
|
|
0.20 mol��L-1KNO3��Һ |
0 |
0 |
0 |
10.0 |
c |
|
|
0.20 mol��L-1(NH4)2SO4��Һ |
0 |
10.0 |
15.0 |
0 |
0 |
|
|
20 ��ʱ����Ӧʱ�䦤t��s�� |
32 |
67 |
130 |
66 |
135 |
|
|
Ϊ��ʹ��Һ������ǿ�Ⱥ���������ֲ��䣬���ٵ�(NH4)2S2O8��Һ��KI��Һ���������ֱ���(NH4)2SO4��Һ��KNO3��Һ���㣻��Һ��Ϻ�������� |
��2��Ϊ��ʹ��Ӧ��ֽ��У�����������ʵ�������Ӧ�ò��Ͻ��еIJ����� ��
��3���ڢ���ʵ���v(S2O82��)= mol��(L��s)-1��
��4�������ϱ����ݷ��������Եõ��Ľ����У�д��һ�����ɣ�
��
II��ʵ��С������ϵ�֪������Na2CO3��Na2S��Һ��ͨ��SO2�������Ʊ�����ʵ�������Na2S2O3����Ӧ���£�Na2CO3 + SO2= Na2SO3 + CO2��2Na2S + 3SO2 = 2Na2SO3 + 3S����
Na2SO3 + S= Na2S2O3����С���������ԭ�������ͼ��ʾװ���Ʊ�Na2S2O3��

��1��ʵ��Ӧ�����к������ŷŵ������С�װ�â١�����ʢ�ŵ��Լ�������
�� ��
�� ��
��2��ʵ������У����������ͨ�룬װ�â��������ݲ��������д�����ɫ��������������ͨ�����壬���Թ۲쵽�������� ��
��3����Ӧ�������Ƶõ�Na2S2O3ϡ��Һ�еõ�Na2S2O3��5H2O�������Ҫ���������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
I��ijУ��ѧʵ��С��̽��Ũ�ȶԻ�ѧ��Ӧ���ʵ�Ӱ�죬���ⶨ![]() ��KI��Ӧ�Ļ�ѧ��Ӧ���ʡ���������ʵ��̽����
��KI��Ӧ�Ļ�ѧ��Ӧ���ʡ���������ʵ��̽����
��ʵ��ԭ����
![]() ��KI��Ӧ�����ӷ���ʽΪ��
��KI��Ӧ�����ӷ���ʽΪ��
![]() ��1��
��1��
ƽ����Ӧ���ʵļ���ʽΪ![]() ��
��
ʵ��ʱ����![]() ��
��![]() �͵���ָʾ�������Һ�м���
�͵���ָʾ�������Һ�м���![]() ��Һ�����Ͻ��衣
��Һ�����Ͻ��衣
�ڷ�Ӧ��1�����е�ͬʱ��������Ӧ��
![]() ��2��
��2��
��Ӧ��1�����ɵ�![]() ������
������![]() ��Ӧ��������ɫ��
��Ӧ��������ɫ��![]() ��
��![]() ��
��![]() �ľ�ʱ����Ӧ��1���������ɵ�
�ľ�ʱ����Ӧ��1���������ɵ�![]() ����������ó�����ɫ���Ӽ���
����������ó�����ɫ���Ӽ���![]() ��Һ��������ɫ��ʱ
��Һ��������ɫ��ʱ
��Ϊ![]() ��
��
��ʵ�����ݡ�
��1��ʵ��С����Ƶ�ʵ���¼�������ݼ�¼���£��뽫������ĸ��ʾ�Ŀո����ϡ�
| ʵ���� | ��[ | �� | �� | �� | �� | |
| �Լ�] ���� ��mL�� | 0��20 mol��L | 20��0 | 10��0 | b | 20��0 | 20��0 |
| 0��20 mol��L | 20��0 | 20��0 | 20��0 | 10��0 | 5��0 | |
| 0��010 mol��L | a | 8��0 | 8��0 | 8��0 | 8��0 | |
| 0��2%������Һ | 2��0 | 2��0 | 2��0 | 2��0 | 2��0 | |
| 0��20 mol��L | 0 | 0 | 0 | 10��0 | c | |
| 0��20 mol��L | 0 | 10��0 | 15��0 | 0 | 0 | |
| 20��ʱ����Ӧʱ�� | 32 | 67 | 130 | 66 | 135 | |
| Ϊ��ʹ��Һ������ǿ�Ⱥ���������ֲ��䣬���ٵģ�NH4��2S2O8��Һ��KI��Һ���������ֱ��ã�NH4��2SO4��Һ��KNO3��Һ���㣻��Һ��Ϻ�������� | ||||||
��2��Ϊ��ʹ��Ӧ��ֽ��У�����������ʵ�������Ӧ�ò��Ͻ��еIJ����� ��
��3���ڢ���ʵ���![]() mol����L��s��
mol����L��s��![]() ��
��
��4�������ϱ����ݷ��������Եõ��Ľ����У�д��һ�����ɣ� ��
 II��ʵ��С������ϵ�֪������NaCO3��Na2S��Һ��ͨ��SO2�������Ʊ�����ʵ�������Na2S2O3����Ӧ���£�
II��ʵ��С������ϵ�֪������NaCO3��Na2S��Һ��ͨ��SO2�������Ʊ�����ʵ�������Na2S2O3����Ӧ���£�
![]()
![]()
![]()
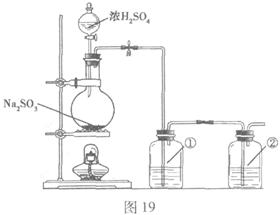
��С���������ԭ�������ͼ19��ʾ
װ���Ʊ�![]() ��
��
��1��ʵ��Ӧ�����к������ŷŵ������С�
װ�â١�����ʢ�ŵ��Լ������Ǣ� ��
�� ��
��2��ʵ������У����������ͨ�룬װ�â����д�����ɫ��������������ͨ�����壬���Թ۲쵽�������� ��
��3����Ӧ�������Ƶõ�![]() ϡ��Һ�еõ�
ϡ��Һ�еõ�![]() �������Ҫ���������� ��
�������Ҫ���������� ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com