
| A、二氧化硅是酸性氧化物,可以与氢氧化钠等强碱溶液反应 |
| B、因为碘易溶于酒精,所以常用酒精萃取碘水中的碘 |
| C、王水、盐酸、水玻璃均为混合物 |
| D、二氧化硅晶体中,1个硅原子与4个氧原子相连 |


 天天向上口算本系列答案
天天向上口算本系列答案科目:高中化学 来源: 题型:
| A、Na+和K+ |
| B、Al3+和Na+ |
| C、Fe2+和NH4+ |
| D、Fe2+和K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、吸热反应不加热就不会发生 |
| B、放热反应不需要加热就能发生 |
| C、键能越大表示物质内所含能量越多 |
| D、化学反应除了生成新物质外,还伴随着能量的变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Cl2通入NaOH溶液:Cl2+OH-→Cl-+ClO-+H2O |
| B、用CH3COOH溶解CaCO3:CaCO3+2H+→Ca2++H2O+CO2↑ |
| C、Cu溶于稀HNO3:3Cu+8H++2NO3-→3Cu2++2NO↑+4H2O |
| D、AlCl3溶液中加入过量稀氨水:Al3++4NH3?H2O→AlO2-+4NH4++2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| n(CH3OH) |
| n(CO2) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、△H1=△H2 |
| B、△H1>△H2 |
| C、△H1<△H2 |
| D、无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
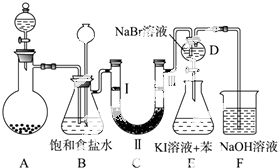 如图是实验室制备氯气并进行一系列相关实验的装置(夹持及加热仪器已略).
如图是实验室制备氯气并进行一系列相关实验的装置(夹持及加热仪器已略).| a | b | c | d | |
| Ⅰ | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| Ⅱ | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
| Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com