
【题目】化合物H是一种药物合成中间体,其合成路线如下:
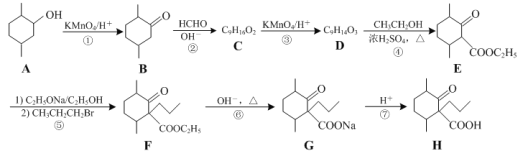
(1)A→B的反应的类型是____反应。
(2)化合物H中所含官能团的名称是______。
(3)化合物C的结构简式为____。B→C反应时会生成一种与C互为同分异构体的副产物,该副产物的结构简式为____。
(4)D的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:____。
①能发生水解反应,所得两种水解产物均含有3种化学环境不同的氢;
②分子中含有六元环,能使溴的四氯化碳溶液褪色。
(5)已知:![]()
![]() CH2ClCH2OH。写出以环氧乙烷(
CH2ClCH2OH。写出以环氧乙烷(![]() )、
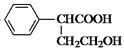
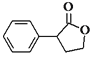
)、![]() 、乙醇和乙醇钠为原料制备
、乙醇和乙醇钠为原料制备 的合成路线流程图____。(无机试剂任用,合成路线流程图示例见本题题干)
的合成路线流程图____。(无机试剂任用,合成路线流程图示例见本题题干)
【答案】氧化 羰基、羧基 

![]()
![]()
![]() CH2ClCH2OH
CH2ClCH2OH 
![]()
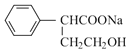
![]()
![]()
【解析】
D→E为酯化反应,则D的结构简式为 ;C与D的碳骨架相同,且C可以与酸性高锰酸钾反应,根据分子式确定含有羟基,故C为
;C与D的碳骨架相同,且C可以与酸性高锰酸钾反应,根据分子式确定含有羟基,故C为 ;A经酸性高锰酸钾氧化,羟基变为羰基,转化为B。B与甲醛在碱性条件下发生加成反应转化为C。E与1-溴丙烷在乙醇/乙醇钠的条件,发生取代反应,脱去一分子HBr,生成F。F在碱性条件下发生水解,酸化得到H。
;A经酸性高锰酸钾氧化,羟基变为羰基,转化为B。B与甲醛在碱性条件下发生加成反应转化为C。E与1-溴丙烷在乙醇/乙醇钠的条件,发生取代反应,脱去一分子HBr,生成F。F在碱性条件下发生水解,酸化得到H。
(1)A→B的反应,醇羟基被氧化为羰基,故反应的类型是氧化反应;
(2)化合物H中所含官能团的名称是羰基、羧基;
(3)根据分析,化合物C的结构简式为 ;B→C反应属于加成,B分子羰基的邻位碳氢键断裂,氢原子与甲醛醛基的氧原子连接,碳原子与甲醛醛基的碳原子连接,但是B羰基由两个邻位,故有两种可能的产物,则生成一种与C互为同分异构体的副产物,该副产物的结构简式为
;B→C反应属于加成,B分子羰基的邻位碳氢键断裂,氢原子与甲醛醛基的氧原子连接,碳原子与甲醛醛基的碳原子连接,但是B羰基由两个邻位,故有两种可能的产物,则生成一种与C互为同分异构体的副产物,该副产物的结构简式为 ;
;
(4)D的一种同分异构体同时满足下列条件①能发生水解反应,说明含有酯基,所得两种水解产物均含有3种化学环境不同的氢,故水解的产物中羧酸部分至少含有三个碳原子,剩下的六个碳原子组成六元环。②分子中含有六元环,能使溴的四氯化碳溶液褪色,说明还有碳碳双键,故可以是![]() ;
;
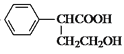
(5)参考E→F的反应,酯基的α-H被卤代烃中的烃基取代从而加长碳链,故合成路线流程图:![]()
![]() CH2ClCH2OH
CH2ClCH2OH 
![]()
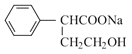
![]()
 。
。


科目:高中化学 来源: 题型:
【题目】A、B、C、D、E都是短周期元素,原子序数依次增大,B、C同周期,A、D同主族。A、B能形成两种常温下的液态化合物甲和乙,原子个数比分别为2∶1和1∶1。根据以上信息回答下列问题:
(1)甲、乙两分子中含有非极性共价键的物质的电子式是________,C元素在周期表中的位置是_____。
(2)C和D的离子中,半径较小的是____(离子符号),以上元素中电负性最大的是____(元素符号)
(3)常温下将D的单质投入甲中,待D消失后再向上述溶液中加入E的固体单质,此时发生反应的化学方程式是______________。
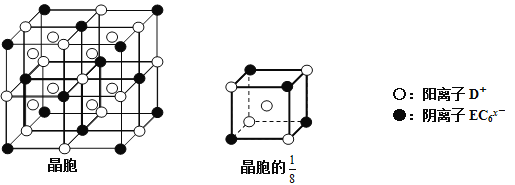
(4)C、D、E可组成离子化合物DxEC6,其晶胞(晶胞是在晶体中具有代表性的最小重复单元)结构如下图所示,阳离子D+(用○表示)位于正方体的棱的中点和正方体内部;阴离子EC6x-(用●表示)位于该正方体的顶点和面心。该化合物的化学式是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以葡萄糖为燃料的微生物燃料电池结构如图所示。已知总反应为C6H12O6+6O2===6CO2+6H2O,关于该电池的叙述正确的是
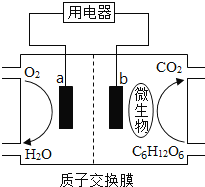
A.a电极反应:O2+2H2O+4e-===4OH-
B.O2在a电极被氧化
C.b电极反应:C6H12O6+6H2O-24e-===6CO2+24H+
D.该电池能够在高温下工作
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制取氨气、收集、验证其还原性并进行尾气处理的装置和原理能达到实验目的的是
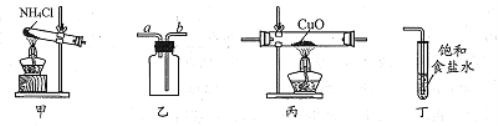
A.用装置甲制取氨气
B.用装置乙收集氨气时气体应该从a口进b口出
C.装置丙中黑色固体变成红色时还原产物一定为铜
D.可以用装置丁吸收氨气,进行尾气处理
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验设计及其对应的离子方程式均正确的是( )
A.用FeCl3溶液腐蚀铜线路板:Cu+2Fe3+→Cu2++2Fe2+
B.Na2O2与H2O反应制备O2:Na2O2+H2O→2Na++2OH-+O2↑
C.将氯气溶于水制备次氯酸:Cl2+H2O→2H++Cl-+ClO-
D.铁与盐酸反应:2Fe + 6H+→2Fe3++3H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五种短周期元素X、Y、Z、M、W的原子序数与其常见化合价的关系如图所示,下列关系不正确的是( )
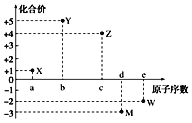
A.元素X可能为锂
B.原子半径大小:r(M)>r(W)
C.X2W中各原子均达到8电子稳定结构
D.元素气态氢化物的稳定性:Y>M
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第3周期某元素的原子,其最外层3p轨道上有一个未成对电子,则关于该元素的描述正确的是( )
A.该元素最高价氧化物的水化物肯定是一种强酸
B.该元素单质可能是一种黄绿色的气体
C.该元素最高价氧化物的水化物肯定是一种强碱,只能与酸反应
D.该元素的原子半径在同周期中肯定是最小的![]() 稀有气体元素除外
稀有气体元素除外![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.1molL-1HCl溶液滴定10.0mL浓度为0.1molL-1Na2CO3溶液,所得滴定曲线如图所示。下列微粒浓度大小关系正确的是
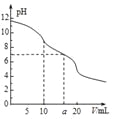
A. 当V=0时:c(H+)+c(HCO3-)+c(H2CO3)=c(OH-)
B. 当V=5时:c(CO32-)+c(HCO3-)+c(H2CO3)=2c(Cl-)
C. 当V=10时:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3)
D. 当V=a时:c(Na+)=c(Cl-)>c(H+)=c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家从化肥厂生产的![]() 中检出组成为
中检出组成为![]() 的物质,经测定,该物质易溶于水,在水中以
的物质,经测定,该物质易溶于水,在水中以![]() 和
和![]() 两种离子形式存在,植物的根系易吸收
两种离子形式存在,植物的根系易吸收![]() ,但它遇到碱时,会生成一种形似白磷的
,但它遇到碱时,会生成一种形似白磷的![]() 分子,
分子,![]() 分子不能被植物吸收。
分子不能被植物吸收。
请回答下列问题:
![]() 和
和![]() 的关系正确的是 ______
的关系正确的是 ______ ![]() 填序号
填序号![]() 。
。
A.同种单质![]() 同位素
同位素![]() 同分异构体
同分异构体![]() 同素异形体
同素异形体
![]() ______
______ ![]() 填“能”或“不能”
填“能”或“不能”![]() 和草木灰混合施用。
和草木灰混合施用。
![]() 已知断裂
已知断裂![]() 吸收167kJ热量,生成1molN
吸收167kJ热量,生成1molN![]() N放出
N放出![]() 的热量,写出
的热量,写出![]() 气体转变为
气体转变为![]() 的热化学方程式: ______ 。
的热化学方程式: ______ 。
![]() 已知白磷、
已知白磷、![]() 、
、![]() 的空间构型均为四面体,
的空间构型均为四面体,![]() 的结构式为
的结构式为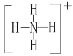 ,白磷
,白磷![]() 的结构式为
的结构式为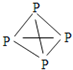 ,请画出
,请画出![]() 的结构式 ______ 。
的结构式 ______ 。
![]() 已知液氨中存在着平衡
已知液氨中存在着平衡![]() ,科学家在液氨中加入氢氧化铯
,科学家在液氨中加入氢氧化铯![]() 和特殊的吸水剂,使液氨中的
和特殊的吸水剂,使液氨中的![]() 生成
生成![]() 分子和另一种单质气体,请写出液氨与氢氧化铯反应的化学方程式: ______ 。
分子和另一种单质气体,请写出液氨与氢氧化铯反应的化学方程式: ______ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com