
下列离子方程式书写正确的是 ( )
A.向氯化铝溶液中通入过量氨气:4NH3+Al3++4H2O===[Al(OH)4]-+4NH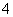
B.将铝片打磨后置于NaOH溶液中:2Al+2OH-+2H2O===2[Al(OH)4]-+H2↑
C.向明矾溶液中加入过量的Ba(OH)2溶液:Al3++2SO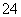 +2Ba2++4OH-===2BaSO4↓+[Al(OH)4]-
+2Ba2++4OH-===2BaSO4↓+[Al(OH)4]-
D.向Na[Al(OH)4]溶液中通入足量CO2:2[Al(OH)4]-+CO2===2Al(OH)3↓+CO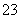 +H2O
+H2O
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
开发、使用清洁能源发展“低碳经济”,正成为科学家研究的主要课题。氢气、甲醇是优质的清洁燃料,可制作燃料电池。
(1)已知:①2CH3OH(1)+ 3O2(g)= 2CO2(g)+ 4H2O(g)ΔH1 = –1275.6 kJ·mol– 1
②2CO(g)+ O2(g)= 2CO2(g) ΔH2 = –566.0 kJ·mol– 1
③H2O(g)= H2O(1) ΔH3 = –44.0 kJ·mol– 1写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式: 。
(2)生产甲醇的原料CO和H2来源于:CH4(g)+ H2O(g)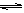 CO(g)+ 3H2(g)
CO(g)+ 3H2(g)
① 一定条件下CH4的平衡转化率与温度、压强的关系如图a。则,Pl P2;A、B、C三点处对应平衡常数(KA、KB、KC)的大小顺序为__________。(填“<”、“>”“=”)
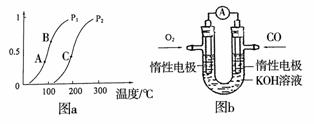
② 100℃时,将1 mol CH4和2 mol H2O通入容积为100 L的反应室,反应达平衡的标志是: 。
a.容器内气体密度恒定
b.单位时间内消耗0.1 mol CH4同时生成0.3 mol H2
c.容器的压强恒定
d.3v正(CH4)= v逆(H2)
如果达到平衡时CH4的转化率为0.5,则100℃时该反应的平衡常数K =
(3)某实验小组利用CO(g)、O2(g)、KOH(aq)设计成如图b所示的电池装置,负极的电极反应式为 。用该原电池做电源,常温下,用惰性电极电解200 mL饱和食盐水(足量),消耗的标准状况下的CO 224 mL,则溶液的pH = 。(不考虑溶液体积的变化)
(4)氢氧燃料电池的三大优点是: 、 、能连续工作。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关说法正确的是( )
A.锂、钛、铁分别位于周期表s、d、ds区
B.CaO的熔点为2614℃,属于原子晶体
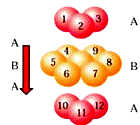
C.金属铬采取体心立方堆积,则其堆积方式如右图
D.某元素的电负性为1.5 ,它是金属元素
查看答案和解析>>
科目:高中化学 来源: 题型:
粉末状试样A是由等物质的量的MgO和Fe2O3组成的混合物。进行如下实验:
①取适量A进行铝热反应,产物中有单质B生成;
②另取20 g A全部溶于0.15 L 6.0 mol·L-1盐酸中,得溶液C;
③将①中得到的单质B和溶液C反应,放出1.12 L(标况)气体,同时生成溶液D,还残留有固体物质B;
④用KSCN溶液检验时,溶液D不变色。
请填空:
(1)①中引发铝热反应的实验操作是________,产物中的单质B是________。
(2)②中所发生的各反应的化学方程式是_____________________________________
________________________________________________________________________。
(3)③中所发生的各反应的离子方程式是_____________________________________
________________________________________________________________________。
(4)若溶液D的体积仍视为0.15 L,则该溶液中c(Mg2+)为__________,c(Fe2+)为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
若甲、乙、丙三位同学用规定的药品制备Al(OH)3。规定必用的药品如下:350 g 70% H2SO4溶液,NaOH固体240 g,足量铝屑、水(不能用其他药品)。
甲、乙、丙用各自设计的方案制得Al(OH)3的质量分别是W1、W2、W3。三种实验方案如下:
甲:铝→加NaOH溶液→加H2SO4溶液→W1 g Al(OH)3
乙:铝→加H2SO4溶液→加NaOH溶液→W2 g Al(OH)3
丙: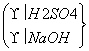 →W3 g Al(OH)3
→W3 g Al(OH)3
试回答:
(1)从充分利用原料、降 低成本和提高产率等因素分析,实验方案最合理的是________。
低成本和提高产率等因素分析,实验方案最合理的是________。
(2)三位学生制得的Al(OH)3,W1、W2、W3其质量由大到小的顺序是________________________________________________________________________。
(3)制得Al(OH)3的最大质量是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上用某种氧化铝矿石(含Fe2O3杂质)为原料冶炼铝的工艺流程如下:
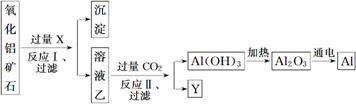
对上述流程中的判断正确的是 ( )
A.试剂X可以为氨水,沉淀中含有铁的化合物
B.CO2可以用H2SO4溶液或稀盐酸代替
C.反应Ⅱ中的反应为CO2+[Al(OH)4]-===Al(OH)3↓+HCO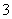
D.工业上还可采用Fe还原Al2O3的方法制Al,成本更低
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是 ( )
A.铝制容器可盛装热的浓硫酸
B.镁的金属性比 铝的金属性强
铝的金属性强
C.氢氧化铝能溶于过量氨水
D.镁在空气中燃烧生成的固体只有MgO
查看答案和解析>>
科目:高中化学 来源: 题型:
A元素的阳离子与B元素的阴离子具有相同的电子层结构,有关两元素的下列叙述:
①原子半径A>B; ②离子半径A>B; ③A的正价与B的负价绝对值一定相等;④电负性A<B; ⑤第一电离能A>B
其中正确的组合是( )
A.①④ B.①②③ C.①④⑤  D.②③⑤
D.②③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
某有机物A的红外光谱和核磁共振氢谱如图所示,下列说法中错误的是( )
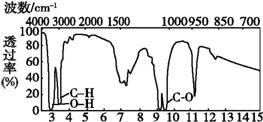
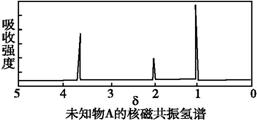
A.由红外光谱可知,该有机物中至少有三种不同的化学键
B.由核磁共振氢谱可知,该有机物分子中有三种不同的氢原子
C.若A的化学式为C2H6O,则其结构简式为CH3-O-CH3
D.仅由其核磁共振氢谱无法得知其分子中的氢原子总数
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com