
【题目】黄铜矿(CuFeS2)是最重要的铜矿,全世界三分之二的铜是由它提炼的。
铜矿冶炼过程中发生的反应有:2CuFeS2+O2=Cu2S+2FeS+SO2 ;2Cu2S+3O2=2Cu2O+2SO2;2Cu2O+Cu2S=6Cu+SO2
回答下列问题:
(1)Cu属于_____区的元素,黄铜矿中铜离子基态外围电子排布式为_____________。
(2)铜矿冶炼过程中产生的SO2可用于生产硫酸,SO2的空间构型为___________,中心原子的杂化方式为__________。冶炼过程还产生了Cu2S 、Cu2O,其中熔点较高的是______________,原因是_______________。
(3)黄铜矿不溶于稀硫酸,但可以溶解在稀硝酸中,硝酸将其中的铁、硫元素氧化到高价态,可以用黄血盐K4[Fe(CN)6]检验Fe3+的存在,1 mol K4[Fe(CN)6]中含有的σ键的数目为_______________。
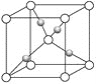
(4)Cu2O晶体的晶胞如图所示,晶胞的密度为ρ g/cm3,阿伏加德罗常数的值为NA,则Cu原子配位数为__________,最近的两个O原子之间的距离为____________nm。
【答案】ds 3d9 V形 sp2 Cu2O 阳离子相同,O2-半径比S2-小,Cu2O晶格能更大,熔点更高 12NA 2 ![]()
【解析】
(1) Cu位于周期表中第4周期第IB族,则基态Cu原子的价电子排布式为3d104s1,据此分析解答;
(2) 根据VSEPR理论, SO2中S的价电子对数为=2+![]() =3;离子晶体熔沸点与晶格能成正比,晶格能与离子半径成反比、与电荷成正比,根据氧离子与硫离子半径大小分析解答;
=3;离子晶体熔沸点与晶格能成正比,晶格能与离子半径成反比、与电荷成正比,根据氧离子与硫离子半径大小分析解答;
(3) K4[Fe(CN)6]中含有C≡N,1个C≡N中有1个σ键,N原子有孤对电子,铁原子有空轨道,所以每个铁离子与CN-形成6个配位键,据此分析解答;
(4)白球的数目=8×![]() +1=2,黑球的数目=4,说明白球为O,黑球为Cu,根据晶胞结构判断Cu原子的配位数;根据晶胞结构图,最近的两个O原子之间的距离为晶胞体对角线的一半,结合晶胞的密度为ρ g/cm3,首先计算晶胞的体积,再求出晶胞的边长,据此解答。
+1=2,黑球的数目=4,说明白球为O,黑球为Cu,根据晶胞结构判断Cu原子的配位数;根据晶胞结构图,最近的两个O原子之间的距离为晶胞体对角线的一半,结合晶胞的密度为ρ g/cm3,首先计算晶胞的体积,再求出晶胞的边长,据此解答。
(1) Cu位于周期表中第4周期第IB族,则基态Cu原子的价电子排布式为3d104s1,属于ds区的元素;铜离子基态外围电子排布式为3d9,故答案为:ds;3d9;
(2) 根据VSEPR理论,对于SO2,价电子对数为=2+![]() =3,根据杂化轨道理论,S原子的杂化方式为sp2,空间构型为V形;离子晶体熔沸点与晶格能成正比,晶格能与离子半径成反比、与电荷成正比,因为氧离子半径小于硫离子半径,所以氧化亚铜的晶格能大于硫化亚铜的晶格能,熔点也高于硫化亚铜,故答案为:V形;sp2;Cu2O;阳离子相同,O2-半径比S2-小,Cu2O晶格能更大,熔点更高;
=3,根据杂化轨道理论,S原子的杂化方式为sp2,空间构型为V形;离子晶体熔沸点与晶格能成正比,晶格能与离子半径成反比、与电荷成正比,因为氧离子半径小于硫离子半径,所以氧化亚铜的晶格能大于硫化亚铜的晶格能,熔点也高于硫化亚铜,故答案为:V形;sp2;Cu2O;阳离子相同,O2-半径比S2-小,Cu2O晶格能更大,熔点更高;
(3) 1mol K4[Fe(CN)6]中含有6molC≡N,1个C≡N中有1个σ键,N原子有孤对电子,铁原子有空轨道,所以每个铁离子与CN-形成6个配位键,即有6个σ键,因此1mol K4[Fe(CN)6]中含有σ键为12mol,数目为12NA,故答案为:12NA;
(4)根据晶胞结构,白球的数目=8×![]() +1=2,黑球的数目=4,根据化学式Cu2O可知,白球为O,黑球为Cu,在每个铜原子周围有2个O原子,即Cu原子配位数为2;1个晶胞的质量=
+1=2,黑球的数目=4,根据化学式Cu2O可知,白球为O,黑球为Cu,在每个铜原子周围有2个O原子,即Cu原子配位数为2;1个晶胞的质量=![]() g,晶胞的密度为ρ g/cm3,则晶胞的体积=
g,晶胞的密度为ρ g/cm3,则晶胞的体积=![]() cm3=
cm3=![]() cm3,晶胞的边长=
cm3,晶胞的边长=![]() cm,根据晶胞结构图,最近的两个O原子之间的距离为晶胞体对角线的一半=
cm,根据晶胞结构图,最近的两个O原子之间的距离为晶胞体对角线的一半=![]() ×
×![]() cm=
cm=![]() ×
×![]() ×107nm,故答案为:2;
×107nm,故答案为:2;![]() ×
×![]() ×107。
×107。


 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案科目:高中化学 来源: 题型:
【题目】下列有关实验操作,说法正确的是
A. 配制一定物质的量浓度溶液时,容量瓶中有少量的水会导致溶液浓度偏低
B. 用盐酸标准溶液滴定未知浓度氨水,选用酚酞做指示剂的结果比甲基橙更准确
C. 测定硫酸铜晶体中结晶水含量时,加热后的坩埚应直接放置在石棉网上冷却
D. 测定中和热时,应迅速将酸、碱稀溶液在有保温措施的容器内混合、搅拌,记录最高温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】自来水是用氯气杀菌消毒的,不法商贩用自来水冒充纯净水销售,为辨别纯净水真伪,可用下列哪种试剂鉴别 ( )
A.酚酞试液 B.氯化铁溶液 C.硝酸银溶液 D.氢氧化钠溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某厂废酸主要含硫酸、Fe3+、Fe2+、TiO2+、Al3+,利用该废液制备过二硫酸铵[(NH4)2S2O8]和TiO(OH)2的一种工艺流程如下:
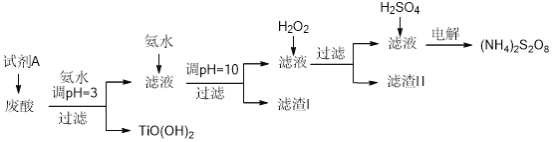
已知:i.
金属离子 | TiO2+ | Fe3+ | Fe2+ | Al3+ |
开始沉淀的pH | 1.2 | 1.9 | 7.0 | 3.2 |
沉淀完全的pH | 2.8 | 3.1 | 9.4 | 4.7 |
ii.pH>7时,Fe2+部分生成Fe(II)氨络离子[Fe(NH3)2]2+。
请回答下列问题:
(1)试剂A为__________,其作用是____________。
(2)取少量TiO(OH)2,用稀盐酸溶解,滴加少量KSCN溶液后无明显现象。再加入少量H2O2,出现微红色。焙烧TiO(OH)2获得的TiO2会发黄,发黄的杂质可能是__________(填化学式)。
(3)滤渣I的主要成分除Fe(OH)2、Al(OH)3外,还含有__________(填化学式)。
(4)加入H2O2的目的是氧化除掉Fe(II)氨络离子[Fe(NH3)2]2+,配平下列离子方程式:2[Fe(NH3)2]2++_____+4H2O+H2O2=______+4NH3·H2O
(5)过二硫酸铵中硫元素的化合价为__________。
(6)常温下,含硫微粒主要存在形式与 pH的关系如下图所示。
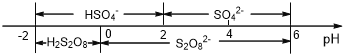
用惰性电极电解饱和NH4HSO4溶液制备过二硫酸铵时,在阳极放电的离子主要为HSO4-,则阳极区电解质溶液的pH范围为____<pH<____,其电极反应式为____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气中NO产生的反应为:N2(g)+O2(g)![]() 2NO(g),一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应,下图曲线a表示该反应在温度T下N2的浓度随时间的变化,曲线b表示该反应在某一起始反应条件改变时N2的浓度随时间的变化。下列叙述正确的是:
2NO(g),一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应,下图曲线a表示该反应在温度T下N2的浓度随时间的变化,曲线b表示该反应在某一起始反应条件改变时N2的浓度随时间的变化。下列叙述正确的是:

A. 温度T下,该反应的平衡常数K=![]()
B. 温度T下,随着反应的进行,混合气体的密度减小
C. 曲线b对应的条件改变可能是加入了催化剂
D. 若曲线b对应的条件改变是温度,可判断该反应的△H<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向300 mL 1 mol·L-1的稀硝酸中,加入5.6 g铁粉,充分反应后,铁粉全部溶解(假设还原产物只有NO),下列说法不正确的是( )
A. 最终所得溶液中既有Fe2+又有Fe3+
B. 最终溶液中,硝酸无剩余
C. 标准状况下生成NO的体积为1.68 L
D. 再向最终所得溶液中滴加稀硝酸,无明显变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生利用以下装置探究喷泉实验.其中A、F分别为硫化氢和氯气的发生装置,C为纯净千燥的氯气与硫化氢反应的装置.打开![]() ,将常温常压下的
,将常温常压下的![]() 控制等体积通入烧瓶且最终气体刚好充满烧瓶.
控制等体积通入烧瓶且最终气体刚好充满烧瓶.
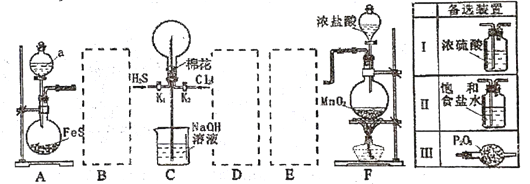
下列说法正确的是:
A. 装置A中的分液漏斗内液体a可选用稀硝酸
B. 虚线框B、D、E内从右上图的“备选装置”中选择合适装置的编号依次为Ⅲ、Ⅱ、Ⅰ
C. 立即看到烧瓶内产生“喷泉”现象
D. 本实验必须对烧瓶冷敷或热敷来引发喷泉
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有甲、乙两位学生利用原电池反应检测金属的活动性顺序,两人都使用镁片与铝片作电极,但甲同学将电极放入6 mol·L-1硫酸溶液中,乙同学将电极放入6 mol·L-1的氢氧化钠溶液中,如下图所示。
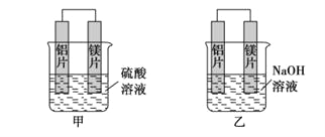
(1)写出甲池中正极的电极反应式_______________________________________。
(2)写出乙池中负极的电极反应式________________________________________。
(3)写出乙池中总反应的离子方程式_______________________________________。
(4)如果甲与乙同学均认为“构成原电池的电极材料如果都是金属,则构成负极材料的金属应比构成正极材料的金属活泼”,则甲会判断出________活动性更强,而乙会判断出________活动性更强(填写元素符号)。
(5)由此实验,可得到如下哪些结论正确(____)
A.利用原电池反应判断金属活动顺序时应注意选择合适的介质
B.镁的金属性不一定比铝的金属性强
C.该实验说明金属活动顺序已过时,已没有实用价值
D.该实验说明化学研究对象复杂、反应受条件影响较大,因此应具体问题具体分析
(6)上述实验也反过来证明了“直接利用金属活动顺序判断原电池中的正负极”这种做法________(可靠或不可靠)。如不可靠,请你提出另一个判断原电池正负极的可行实验方案________________(如可靠,此空可不填)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间有如下转化关系: 下列有关物质的推断不正确的是 ( )
下列有关物质的推断不正确的是 ( )
A. 若甲为AlC13溶液,则丁可能是NaOH溶液 B. 若甲为N2,则丁可能是O2
C. 若甲为Fe,则丁可能是稀硝酸 D. 若甲为NaOH溶液,则丁可能是CO2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com