
在T℃时,将a g NH3完全溶于水,得到V mL溶液,假设该溶液的密度为ρ g/cm3,溶质的质量分数为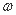 ,物质的量浓度为c mol·L-1。则下列选项不正确的是
,物质的量浓度为c mol·L-1。则下列选项不正确的是
A.溶质的质量分数为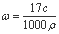
B.用水稀释该溶液,OH- 的物质的量增加
C.该溶液中共有6种微粒
D.上述溶液中再加入V mL水后,所得溶液溶质的质量分数大于0.5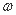
【知识点】物质的量浓度的相关计算;溶液中溶质的质量分数及相关计算 A4
【答案解析】D 解析:A.氨水溶液溶质为氨气,设该溶液的体积为1L,所以溶液质量为1000ρg,溶质氨气的质量为17cg,溶质的质量分数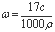 ,故A正确;
,故A正确;
B.用水稀释该溶液,溶液中的一水合氨的电离程度增大故OH- 的物质的量增加,故B正确;
C、该溶液中含有NH4+ 、OH-、H+、NH3、H2O和NH3·H2O6种微粒,正确;
D.水的密度比氨水的密度大,相等体积的氨水与水,水的质量大,等体积混合后溶液的质量大于原氨水的2倍,溶液中氨气的质量相同,根据溶质的质量分数=m(溶质)/ m(溶液)×100%可知,等体积混合所得溶液溶质的质量分数小于0.5ω,故D错误。
【思路点拨】本题考查了溶液浓度的相关计算,同时也涉及到了电离平衡、弱电解质的电离问题,综合性较强。


 优学名师名题系列答案
优学名师名题系列答案科目:高中化学 来源: 题型:
如图
 (1)图I表示10mL量筒中液面的位置,A与B、B与C刻度相差1mL,如果刻度A为5,量筒中液体体积是 mL。
(1)图I表示10mL量筒中液面的位置,A与B、B与C刻度相差1mL,如果刻度A为5,量筒中液体体积是 mL。
(2)图II表示25mL滴定管中液面的位置,如果液面处的读数是a,则滴定管中液体的体积(填代号) 。
A.是a mL B.是(25-a)mL
C.一定大于a mL D.一定大于(25-a)mL
(3)写出下列物质的水解离子方程式
NaClO溶液: Fe2 (SO4)3 溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
在标准状况下,将V L  A气体(摩尔质量是M g/mol)溶于0.1 L水中,所得溶液的密度为d g/cm3,则此溶液的物质的量浓度为 ( )
A气体(摩尔质量是M g/mol)溶于0.1 L水中,所得溶液的密度为d g/cm3,则此溶液的物质的量浓度为 ( )
A.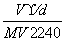 B.
B.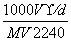
C.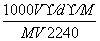
 D.
D.
查看答案和解析>>
科目:高中化学 来源: 题型:
下列哪些量为已知条件时,可用于求物 质的量浓度?先找出有关组合(填代号),再写出由这些量求物质的量浓度的计算式(每种情
质的量浓度?先找出有关组合(填代号),再写出由这些量求物质的量浓度的计算式(每种情 况最多只能选择三个量)。
况最多只能选择三个量)。
①溶液体积V(L) ②溶液的密度d(g·mL-1) ③溶质的摩尔质量M(g·mol-1)
④溶质的质量分数w ⑤溶质的质量m(g) ⑥气态溶质在标准状况下的体积V′(L)
第一种情况:已知________,则c=________mol·L-1;
第二种情况:已知________,则c=________mol·L-1;
第三种情况:已知________,则c=________mol·L-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
利用实验器材(规格和数量不限)能够完成相应实验的一项是
| 选项 | 实验器材(省略夹持装置) | 相应实验 |
| A | 三脚架、泥三角、坩埚、坩埚钳 | 煅烧石灰石制取生石灰 |
| B | 烧杯、玻璃棒、胶头滴管、100 mL容量瓶 | 用浓盐酸配制100mL 0.1 mol·L-1的稀盐酸溶液 |
| C | 烧杯、玻璃棒、分液漏斗 | 用饱和Na2CO3溶液除去乙酸乙酯中的乙酸和乙醇 |
| D | 烧杯、酸式滴定管、碱式滴定管 | 用H2SO4标准液滴定未知浓度的NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
分类是化学研究中常用的方法.下列分类方法中,不正确的是 ( )
A.依据分子组成中含有氢原子的数目,将酸分为一元酸、二元酸等
B.依据是否有电子转移,将化学反应分为氧化还原反应和非氧化还 原反应
原反应
C.依据能量的变化,将化学反应分为放热反应和吸热反应
D.依据组成元素的种类,将纯净物分为单质和化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于胶体和溶液的说法中,正确的是 ( )
A.胶体不均一、不稳定,静置后易产生沉淀;溶液均一、稳定,静置后不产生沉淀
B.布朗运动是胶体粒子特有的运动方式,可以据此把胶体与溶液、悬浊液区分
C.光线通过时,胶体产生丁达尔效应,溶液则无丁达尔效应
D.只有胶状的物质如胶水、果冻类的才能称为胶体
查看答案和解析>>
科目:高中化学 来源: 题型:
在2 L密闭容器内,800℃时反应2NO(g)+O2(g)  2NO2(g)体系中,
2NO2(g)体系中, n(NO)随时间的变化如表:
n(NO)随时间的变化如表:
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)写出该反应的平衡常数表达式:K=__________.已知:K300℃>K350℃,则该反应是________热反应.
(2)图中表示NO2的变化的曲线是________.用O2表示从0~2 s内该反应的平均速率v=________.

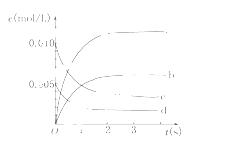
(3)能说明该反应已达到平衡状态的是________.
a.v(NO2)=2v(O2)
b.容器内压强保持不变
c.v逆(NO)=2v正(O2)
d.容器内密度保持不变
(4)能使该反应的反应速率增大,且平衡向正反应方向移动的是________.
a.及时分离出NO2气体
b.适当升高温度
c.增大O2的浓度
d.选择高效催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
洗涤下列试管时,选用的试剂(括号中物质)不妥当的是 ( )
A.做过KMnO4分解反应实验的试管(浓盐酸)
B.做过木炭还原氧化铜实验的试管( 硝酸)
硝酸)
C.做过银镜反应实验的试管(氨水)
D.做过Na2S2O3与稀硫酸反应的试管(二硫化碳)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com