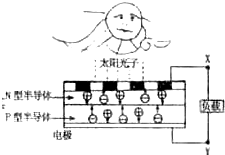
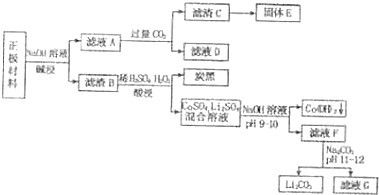
某化学小组在进行知识整理时发现如下规律:有些反应随着浓度由浓变稀,可能导致“量变引起质变”,并据此拟定了如下几个相关题目,请你给出相应答案(不必写求解过程).
(1)实验室制取氯气的化学方程式为MnO
2+4HCl(浓)
MnCl
2+Cl
2↑+2H
2O(MnO
2不能氧化稀盐酸).用下列两种方法制取氯气:①用含HCl146g的浓盐酸与足量MnO
2充分反应;②用87gMnO
2与足量的浓盐酸充分反应.不考虑HCl 挥发,则两种方法生成的氯气的量的是方法①
<
<
(填“>”、“<”或“=”)方法②.
(2)写出铜与浓硫酸在加热条件下反应的化学方程式
Cu+2H
2SO
4(浓)
CuSO
4+SO
2↑+2H
2O
Cu+2H
2SO
4(浓)
CuSO
4+SO
2↑+2H
2O
.
用100mL、18.0mol?L
-1的浓硫酸与足量的铜反应后,被还原的硫酸的物质的量
<
<
(填“>”、“<”或“=”)0.900mol.
(3)25.6g铜投入到100mL、12.0mol?L
-1的浓硝酸中,起初发生的反应的化学方程式为
Cu+4HNO3=Cu(NO3)2+2NO2↑+2H2O
Cu+4HNO3=Cu(NO3)2+2NO2↑+2H2O
.一段时间后两种物质恰好完全反应.若生成的气体只有NO、NO
2两种成分,其在标准状况下的总体积为
8.96L
8.96L
.

 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案