
ŅŃÖŖA”¢B”¢C”¢D”¢E”¢FŹĒŗ¬ÓŠĶ¬Ņ»ÖÖŌŖĖŲµÄ»ÆŗĻĪļ£¬ĘäÖŠFŹĒÄÜŹ¹ŹŖČóŗģÉ«ŹÆČļŹŌÖ½±äĄ¶µÄĘųĢ壬ĖüĆĒÖ®¼äÄÜ·¢ÉśČēĻĀ·“Ó¦£ŗ¢ŁA+H2O”śB+C””¢ŚC+F”śD””¢ŪD+NaOH F+E+H2O
F+E+H2O
£Ø1£©Š“³öĖüĆĒµÄ»ÆѧŹ½£ŗA”””””¢B”””””¢C”””””¢D”””””¢E”””””¢F””””£»
£Ø2£©Š“³öø÷²½·“Ó¦µÄ»Æѧ·½³ĢŹ½£¬²¢Öø³ö·“Ó¦¢ŁµÄŃõ»Æ¼ĮŗĶ»¹Ō¼Į£®
¢Ł””””£¬Ńõ»Æ¼Į”””””¢»¹Ō¼Į””””£®
¢Ś””””£®
¢Ū””””£®
£Ø3£©¹¤ŅµÉś²śCµÄ¹ż³ĢÖŠÓŠČēĻĀŅ»²½·“Ó¦£¬¼“F¾“ß»ÆŃõ»ÆÉś³ÉBŗĶH2O£¬Š“³öøĆ²½·“Ó¦µÄ»Æѧ·½³ĢŹ½””””£®
| ĪŽ»śĪļµÄĶʶĻ£® | |
| ·ÖĪö£ŗ | A”¢B”¢C”¢D”¢E”¢FŹĒŗ¬ÓŠĶ¬Ņ»ÖÖŌŖĖŲµÄ»ÆŗĻĪļ£¬F¾“ß»ÆŃõ»ÆÉś³ÉBŗĶH2O£¬ŌņFŹĒNH3£¬ĖüĆĒÖ®¼äÄÜ·¢ÉśČēĻĀ·“Ó¦£ŗ¢ŪD+NaOH”śF+E+H2O£¬ĖµĆ÷DŹĒļ§ŃĪ£¬EĪŖÄĘŃĪ£¬ĒŅA”¢B”¢C”¢D”¢E”¢FŹĒŗ¬ÓŠĶ¬Ņ»ÖÖŌŖĖŲµÄ»ÆŗĻĪļ£¬ŌņEŹĒNaNO3£¬DŹĒNH4NO3£¬øł¾Ż¢ŚC+F”śDÖŖ£¬CŹĒHNO3£¬øł¾Ż¢ŁA+H2O”śB+CÖŖ£¬ĒŅAŗĶB”¢C¶¼ŗ¬ÓŠĶ¬Ņ»ÖÖŌŖĖŲ£¬ŌņAŹĒNO2£¬BŹĒNO£¬øł¾ŻĪļÖŹµÄŠŌÖŹ·ÖĪö½ā“š£® |
| ½ā“š£ŗ | ½ā£ŗ½ā£ŗA”¢B”¢C”¢D”¢E”¢FŹĒŗ¬ÓŠĶ¬Ņ»ÖÖŌŖĖŲµÄ»ÆŗĻĪļ£¬F¾“ß»ÆŃõ»ÆÉś³ÉBŗĶH2O£¬ŌņFŹĒNH3£¬ĖüĆĒÖ®¼äÄÜ·¢ÉśČēĻĀ·“Ó¦£ŗ¢ŪD+NaOH”śF+E+H2O£¬ĖµĆ÷DŹĒļ§ŃĪ£¬EĪŖÄĘŃĪ£¬ĒŅA”¢B”¢C”¢D”¢E”¢FŹĒŗ¬ÓŠĶ¬Ņ»ÖÖŌŖĖŲµÄ»ÆŗĻĪļ£¬ŌņEŹĒNaNO3£¬DŹĒNH4NO3£¬øł¾Ż¢ŚC+F”śDÖŖ£¬CŹĒHNO3£¬øł¾Ż¢ŁA+H2O”śB+CÖŖ£¬ĒŅAŗĶB”¢C¶¼ŗ¬ÓŠĶ¬Ņ»ÖÖŌŖĖŲ£¬ŌņAŹĒNO2£¬BŹĒNO£¬ £Ø1£©ÓÉÉĻ·ÖĪö£¬AĪŖNO2£¬BĪŖNO£¬CĪŖHNO3£¬DĪŖNH4NO3£¬EĪŖNaNO3£¬FĪŖNH3£¬¹Ź“š°øĪŖ£ŗNO2£»NO£»HNO3£»NH4NO3£»NaNO3£»NH3£» £Ø2£©¢Ł¶žŃõ»ÆµŖŗĶĖ®·“Ӧɜ³ÉŅ»Ńõ»ÆµŖŗĶĻõĖį£¬»Æѧ·½³ĢŹ½ĪŖ£ŗ3NO2+H2O=2HNO3+NO£¬øĆ·“Ó¦ÖŠNŌŖĖŲ»ÆŗĻ¼ŪÓÉ+4¼Ū±äĪŖ+2¼ŪŗĶ+5¼Ū£¬ĖłŅŌ“Ė·“Ó¦ÖŠŃõ»Æ¼ĮNO2£¬»¹Ō¼ĮŹĒNO2£¬¹Ź“š°øĪŖ£ŗ3NO2+H2O=2HNO3+NO£»NO2£»NO2£» ¢ŚĪŖĻõĖįÓė°±Ęų·“Ó¦£¬·½³ĢŹ½ĪŖHNO3+NH3=NH4NO3£¬¹Ź“š°øĪŖ£ŗHNO3+NH3=NH4NO3£» ¢ŪĪŖĻõĖįļ§ÓėĒāŃõ»ÆÄĘ·“Ó¦£¬·½³ĢŹ½ĪŖNH4NO3+NaOH=NaNO3+NH3+H2O£¬¹Ź“š°øĪŖ£ŗNH4NO3+NaOH=NaNO3+NH3+H2O£» £Ø3£©¼“NH3¾“ß»ÆŃõ»ÆÉś³ÉNOŗĶH2O£¬·“Ó¦·½³ĢŹ½ĪŖ£ŗ4NH3+5O2 |
| µćĘĄ£ŗ | ±¾ĢāŅŌNŌŖĖŲĪŖŌŲĢåæ¼²éĮĖŗ¬µŖ»ÆŗĻĪļµÄĶʶĻ£¬ŅŌFĪŖĶ»ĘĘæŚ½įŗĻĪļÖŹ¼äµÄ×Ŗ»Æ·ÖĪöĶʶĻ£¬ÄŃ¶Č²»“ó£¬×¢Ņā¶ą×ܽį¹éÄÉ»ł“”ÖŖŹ¶£¬ÖŖµĄ³£¼ūĪļÖŹµÄŠŌÖŹ£® |


 Š”ѧæĪŹ±ĢŲѵĻµĮŠ“š°ø
Š”ѧæĪŹ±ĢŲѵĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ijæĪĶāŠĖȤŠ”×éĪŖĢ½¾æijÖÖĀĮŗĻ½š£ØŗĻ½šŌŖĖŲĪŖMg ŗĶAl£©ŹĒ·ń·ūŗĻ¹ś¼ŅÖŹĮæ±ź×¼£Ø¹ś¼Ņ¹ę¶ØĘäÖŠĀĮŗ¬Įæ²»ÄܵĶÓŚ78£„£©£¬Éč¼ĘĻĀĶ¼×°ÖĆ½ųŠŠŹµŃ锣
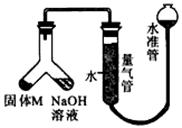
£Ø1£©ČēŗĪ¼ģŃéøĆ×°ÖƵÄĘųĆÜŠŌ ”£
£Ø2£©ŗĻ½šŃłĘ·¹ĢĢåMÓėĒāŃõ»ÆÄĘČÜŅŗ·“Ó¦µÄĄė×Ó·½³ĢŹ½ ”£
£Ø3£©·“Ó¦Ē°ĻȵŚŅ»“Ī¶ĮČ”ĮæĘų¹ÜŅŗĆęæĢ¶Č£¬Č»ŗóĒ抱×ó±ß×°ÖĆŹ¹ĒāŃõ»ÆÄĘČÜŅŗ(×ćĮæ)Óėa gŗĻ½š·ŪÄ©(¹ĢĢåM)³ä·Ö·“Ó¦£¬“ż·“Ó¦Ķ£Ö¹ŗó£¬ĘųĢåĪĀ¶Č»Öø“µ½ŹŅĪĀ£¬ĻėŅŖµŚ¶ž“Ī¶ĮČ”ĮæĘų¹ÜŅŗĆęæĢ¶ČĒ°ŠčŅŖ½ųŠŠµÄŅ»²½²Ł×÷ŹĒ ”£Ķعż¶ĮČ”ŅŗĆę²ī£¬²¢½«ĘųĢåĢå»żÕŪĖć³É±ź×¼×“æöĻĀĢå»żĪŖV mL”£ČōĮæĘų¹Ü×ī“óĮæ³ĢĪŖ50 mL£¬Ōņ¹ĢĢåMÖŠĀĮµÄÖŹĮæ(mA1)·¶Ī§ĪŖ ”£
£Ø4£©Čōa£½38 mg£¬V£½44.8 mL(±ź×¼×“æö)£¬ĒėĶعż¼ĘĖćĖµĆ÷øĆŗĻ½šŹĒ·ń·ūŗĻ¹ś¼Ņ±ź×¼ (Ģī”°·ūŗĻ”±»ņ”°²»·ūŗĻ”±)”£
£Ø5£©Čō½«×°ÖĆÖŠµÄĒāŃõ»ÆÄĘČÜŅŗĢę»»ĪŖ×ćĮæµÄŃĪĖį£¬Ōņ·“Ó¦Ķ£Ö¹ŗóĮæĘų¹ÜÄŚĘųĢåĢå»ż (Ģī”°£¾”±”°£¼”±”°£½”±)V mL”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠĆčŹöÖŠ£¬²»·ūŗĻÉś²śŹµ¼ŹµÄŹĒ( )
A£®µē½āČŪČŚµÄŃõ»ÆĀĮÖĘČ”½šŹōĀĮ£¬ÓĆĢś×÷Ńō¼«
B£®µē½ā·Ø¾«Į¶“ÖĶ£¬ÓĆ“æĶ×÷Ņõ¼«
C£®µē½ā±„ŗĶŹ³ŃĪĖ®ÖĘÉÕ¼ī£¬ÓĆĶæÄųĢ¼øÖĶų×÷Ņõ¼«
D£®ŌŚ¶Ę¼žÉĻµē¶ĘŠæ£¬ÓĆŠæ×÷Ńō¼«
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
230ThŗĶ232ThŹĒīŹµÄĮ½ÖÖĶ¬Ī»ĖŲ£¬232ThæÉŅŌ×Ŗ»Æ³É233U£®ĻĀĮŠÓŠ¹ŲThµÄĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
| ”” | A£® | ThŌŖĖŲµÄÖŹĮæŹżŹĒ232 | B£® | ThŌŖĖŲµÄĻą¶ŌŌ×ÓÖŹĮæŹĒ231 |
| ”” | C£® | 232Th×Ŗ»Æ³É233UŹĒ»Æѧ±ä»Æ | D£® | 230ThŗĶ232ThµÄ»ÆѧŠŌÖŹĻąĶ¬ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ÄÜŌŚČÜŅŗÖŠ“óĮæ¹²“ęµÄŅ»×éĄė×ÓŹĒ£Ø””””£©
| ”” | A£® | NH4+”¢Ag+”¢PO43﹣”¢Cl﹣ | B£® | Fe3+”¢H+”¢I﹣”¢HCO3﹣ |
| ”” | C£® | K+”¢Na+”¢NO3﹣”¢MnO4﹣ | D£® | Al3+”¢Mg2+”¢SO42﹣”¢CO32﹣ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
³£ĪĀĻĀ£¬ĻĀĮŠø÷×éĄė×ÓŌŚÖʶØČÜŅŗÖŠŅ»¶ØÄÜ“óĮæ¹²“ęµÄŹĒ ( )
A£®³ĪĒåĶøĆ÷µÄČÜŅŗÖŠ£ŗCu2£«”¢Mg2£«”¢SO42£”¢Cl£
B£®c(Fe3£«)=0.1mol”¤L”„1µÄČÜŅŗÖŠ£ŗNa£«”¢NH4£«”¢SCN£”¢SO42£
C£®¼ÓČėĀĮ·ŪÄܲśÉśĒāĘųµÄČÜŅŗÖŠ£ŗNH4£«”¢Fe2£«”¢SO42£”¢NO3£
D£®0.1mol”¤L”„1NaHCO3ČÜŅŗÖŠ£ŗK£«”¢Ba2£«”¢OH£”¢Cl£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
Al”¢Fe”¢Cu¶¼ŹĒÖŲŅŖµÄ½šŹōŌŖĖŲ”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
A. ČżÕߵĵ„ÖŹ·ÅÖĆŌŚ³±ŹŖµÄæÕĘųÖŠ¾łÖ»Éś³ÉŃõ»ÆĪļ
B. ÖʱøAlCl3”¢FeCl3”¢CuCl2¾łæÉÓĆĮ½ÖÖµ„ÖŹÖ±½Ó»ÆŗĻµÄ·½·Ø
C. ČżÕ߶ŌÓ¦µÄŃõ»ÆĪļ¾łĪŖ¼īŠŌŃõ»ÆĪļ
D. ČżÕ߶ŌÓ¦µÄĒāŃõ»ÆĪļ¾łæÉÓÉĘä¶ŌÓ¦µÄŃõ»ÆĪļ¼ÓĖ®Éś³É
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ÉčNAĪŖ°¢·ü¼ÓµĀĀŽ³£ŹżµÄÖµ£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
| ”” | A£® | 1L 1mol•L©1µÄNaClO ČÜŅŗÖŠŗ¬ÓŠClO©µÄŹżÄæĪŖNA |
| ”” | B£® | ±ź×¼×“æöĻĀ£¬Ņ»¶ØĮæµÄĶÓėĻõĖį·“Ó¦ŗóÉś³É22.4 L NO”¢NO2”¢N2O4µÄ»ģŗĻĘųĢ壬Ōņ±»»¹ŌµÄĻõĖįµÄ·Ö×ÓŹż“óÓŚNA |
| ”” | C£® | Ģś×öµē¼«µē½āŹ³ŃĪĖ®£¬ČōŅõ¼«µĆµ½NAøöµē×Ó£¬ŌņŃō¼«²śÉś11.2LĘųĢå£Ø±źæöĻĀ£© |
| ”” | D£® | ±ź×¼×“æöĻĀ£¬6.72L NO2ÓėĖ®³ä·Ö·“Ó¦×ŖŅʵĵē×ÓŹżÄæĪŖ0.1NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ij»ÆѧŠĖȤŠ”×éŌŚŹµŃéŹŅĢõ¼žĻĀŅŌĮņĖįĶČÜŅŗĪŖµē½āŅŗ£¬ÓƵē½āµÄ·½·ØŹµĻÖĮĖ“ÖĶ(ŗ¬ÓŠÉŁĮæµÄŠæ”¢Ģś”¢Ņų”¢½šµČ½šŹōŗĶÉŁĮææóĪļŌÓÖŹ)µÄĢį“棬²¢¶ŌŃō¼«ÄąŗĶµē½āŅŗÖŠ½šŹō½ųŠŠ»ŲŹÕŗĶŗ¬Įæ²ā¶Ø”£Ēė»Ų“šŅŌĻĀĪŹĢā”£
£Ø1£©µē½āŹ±£¬“ÖĶÓ¦ÓėµēŌ“µÄ ¼«ĻąĮ¬£¬Ņõ¼«ÉĻµÄµē¼«·“Ó¦Ź½ĪŖ £»µē½ā¹ż³ĢÖŠ£¬ĮņĖįĶµÄÅØ¶Č»į (Ń”Ģī”°±ä“ó”±”°²»±ä”±»ņ”°±äŠ””±)”£
£Ø2£©µē½āĶź³Éŗó£¬øĆŠ”×éĶ¬Ń§½«µē½āŅŗ¹żĀĖŗó¶ŌĀĖŅŗŗĶŃō¼«Äą·Ö±š½ųŠŠ“¦Ąķ£ŗ
¢ŁŃō¼«ÄąµÄ×ŪŗĻĄūÓĆ£ŗĻ”ĻõĖį“¦ĄķŃō¼«ÄąµĆµ½ĻõĖįŅųĻ”ČÜŅŗ£¬ĒėÄ抓³öøĆ²½·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ ”£
¢ŚCuµÄ»ŲŹÕ”¢ĀĖŅŗ³É·Ö¼°ŗ¬ĮæµÄ²ā¶Ø£ŗŅŌĻĀŹĒøĆŠ”×éÉč¼ĘµÄŅ»øöŹµŃéĮ÷³Ģ”£
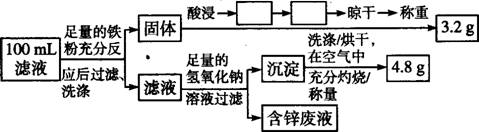
ŌŚÉĻŹöĮ÷³ĢÖŠæÕøńÄŚĢīÉĻĻąÓ¦µÄ²Ł×÷£ŗ ”¢ £»100 mLĀĖŅŗÖŠCu2+µÄÅضČĪŖ mol/l£¬Fe2+µÄÅضČĪŖ mol/l”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com