
| 10-11 |
| 10-3 |
| 1 |
| 108 |
| 1 |
| 108 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ʵ����� | ��������/g | ������̬ | c��H2SO4�� /mol?L-1 |
V��H2SO4�� /mL |
��Һ�¶� | ������ʧ��ʱ��/s | |
| ��Ӧǰ | ��Ӧ�� | ||||||
| 1 | 0.10 | ��Ƭ | 0.7 | 50 | 20 | 36 | 250 |
| 2 | 0.10 | ��Ƭ | 0.8 | 50 | 20 | 35 | 200 |
| 3 | 0.10 | ���� | 0.8 | 50 | 20 | 36 | 25 |
| 4 | 0.10 | ��Ƭ | 1.0 | 50 | 20 | 35 | 125 |
| 5 | 0.10 | ��Ƭ | 1.0 | 50 | 35 | 50 | 20 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A�� ֤�����ԣ����̼����� |
B�� ʯ������ |
C�� ʵ������������ |
D�� ʵ�������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
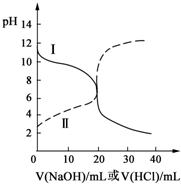 25��ʱ��ȡŨ�Ⱦ�Ϊ0.1mol?L-1�Ĵ�����Һ�Ͱ�ˮ��Һ��20mL���ֱ���0.1mol?L-1NaOH��Һ��0.1mol?L-1��������к͵ζ����ζ�������pH��μ���Һ������仯��ϵ��ͼ��ʾ������˵����ȷ���ǣ�������
25��ʱ��ȡŨ�Ⱦ�Ϊ0.1mol?L-1�Ĵ�����Һ�Ͱ�ˮ��Һ��20mL���ֱ���0.1mol?L-1NaOH��Һ��0.1mol?L-1��������к͵ζ����ζ�������pH��μ���Һ������仯��ϵ��ͼ��ʾ������˵����ȷ���ǣ�������| A�����ߢμ���Һ��10mLʱ��c��CH3COO-����c��Na+����c��H+����c��OH-�� |
| B�����ߢμ���Һ��20 mLʱ��c��Cl-����c��NH4+����c��H+����c��OH-�� |
| C�����ߢμ���Һ��10 mL��20 mL֮����ڣ�c��NH4+��=c��Cl-����c��OH-��=c��H+�� |
| D�����ߢμ���Һ��10 mLʱ��c��CH3COO-��-c��CH3COOH��=2[c��H+��-c��OH-��] |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| 1 |
| 2 |
| A���ﵽƽ�����ֻ�����¶ȣ���ѧƽ�������ƶ� |
| B���ﵽƽ�����ͨ��ϡ�����壬�淴Ӧ�������� |
| C��ʹ�ô�����ƽ�ⳣ������ |
| D��0��5min�ڣ�NO�ķ�Ӧ����Ϊ2.4��10-3mol?L-1?min-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| Fe2O3 | CO | Fe | CO2 | |
| ��/mol | 1.0 | 1.0 | 1.0 | 1.0 |
| ��/mol | 1.0 | 2.0 | 1.0 | 1.0 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����״����2.24 L H2O�У�������Ϊ0.1NA |
| B��1 L 0.5mol?L-1 AlCl3��Һ�к��е�Al3+��Ϊ0.5 NA |
| C�����³�ѹ��16g O2�У���ԭ����ΪNA |
| D��0.1mol �����������������ַ�Ӧ��ת�Ƶĵ�����Ϊ0.3NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 �ס��ҡ����������ֵ����ڵ�ȼ������������������X��Y��Z��W���ֻ����ת����ϵ��ͼ��ʾ����֪���ټס��ҡ�����Ϊǰ������Ԫ�صĵ��ʣ������¾�Ϊ��̬�������ճ������е�һ�ֳ����������ڳ����£�X����ɫҺ�壬Y�Ǻ�ɫ���壻�۱�������ȼ�շ�����ɫ���棬��������ȼ�������ػ�ɫ���̣�W��ˮ��Һ�ʻ�ɫ����ش�
�ס��ҡ����������ֵ����ڵ�ȼ������������������X��Y��Z��W���ֻ����ת����ϵ��ͼ��ʾ����֪���ټס��ҡ�����Ϊǰ������Ԫ�صĵ��ʣ������¾�Ϊ��̬�������ճ������е�һ�ֳ����������ڳ����£�X����ɫҺ�壬Y�Ǻ�ɫ���壻�۱�������ȼ�շ�����ɫ���棬��������ȼ�������ػ�ɫ���̣�W��ˮ��Һ�ʻ�ɫ����ش��鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com