
 ��A�������������Se�����ڣ�Te����Ԫ���ڻ������г����ֳ���������̬������A��Ԫ�صĻ��������о�����������������Ҫ��;����ش��������⣺
��A�������������Se�����ڣ�Te����Ԫ���ڻ������г����ֳ���������̬������A��Ԫ�صĻ��������о�����������������Ҫ��;����ش��������⣺���� ��1������ͼƬ֪��ÿ��Sԭ�Ӻ���2���Ҽ���2���µ��Ӷԣ����ݼ۲���ӶԻ�������ȷ��Sԭ���ӻ���ʽ��
��2��ͬһ����Ԫ�أ�Ԫ��ԭ��ʧ������������ԭ���������������ǿ��ԭ��ʧ��������Խǿ�����һ������ԽС��
��3��SeԪ��34��Ԫ�أ�M���Ӳ�����18�����ӣ��ֱ�λ��3s��3p��3d�ܼ��ϣ�
��4���ǽ�����Խǿ��Ԫ�أ�������Ԫ�صĽ������Խǿ�������⻯����ˮ��Һ�о�Խ�ѵ��룬���Ծ�Խ����
���ݼ۲���ӶԻ�������ȷ����̬SeO3���ӵ����幹�͡�SO32-���ӵ����幹�ͣ�
��5���ٵ�һ����������ɵĸ����ӣ������ٽ�һ�������������ɵ������ӣ�
�ڸ�������Ԫ��Se�Ļ��ϼۿ����жϵ��Ըߵͣ�����Խ�ߣ���Se-O-H��Oԭ�ӵĵ�������Խǿ��Խ�����H+��
��6�����þ�̯�����㾧����Zn��Sԭ����Ŀ���������㾧���������ٸ��ݦ�=$\frac{m}{V}$���㾧���ܶȣ�
bλ�ú�ɫ������Χ4����ɫ����������ṹ����ɫ����������ɫ�����н�Ϊ109��28�䣬����aλ�ð�ɫ�������İ�ɫ����룬��aλ��S2-��bλ��Zn2+֮��ľ��룬�����������������ߡ��н�������߹�ϵ��a2+b2-2abcos��=c2���㣮
��� �⣺��1������ͼƬ֪��ÿ��Sԭ�Ӻ���2���Ҽ���2���µ��Ӷԣ�����ÿ��Sԭ�ӵļ۲���ӶԸ�����4����Sԭ��Ϊsp3�ӻ����ʴ�Ϊ��sp3��
��2��ͬһ����Ԫ�أ�Ԫ��ԭ��ʧ������������ԭ���������������ǿ��ԭ��ʧ��������Խǿ�����һ������ԽС���������һ�����ܴ�С˳����O��S��Se���ʴ�Ϊ��O��S��Se��
��3��SeԪ��34��Ԫ�أ�M���Ӳ�����18�����ӣ��ֱ�λ��3s��3p��3d�ܼ��ϣ����������M����ӵ��Ų�ʽΪ3s23p63d10���ʴ�Ϊ��34��3s23p63d10��
��4���ǽ�����Խǿ��Ԫ�أ�������Ԫ�صĽ������Խǿ�������⻯����ˮ��Һ�о�Խ�ѵ��룬���Ծ�Խ�����ǽ�����S��Se������H2Se�����Ա�H2Sǿ����̬SeO3������Seԭ�Ӽ۲���ӶԸ�����3�Ҳ����µ��Ӷԣ����������幹��Ϊƽ�������Σ�SO32-������Sԭ�Ӽ۲���ӶԸ���=3+$\frac{1}{2}$��6+2-3��2��=4�Һ���һ���µ��Ӷԣ����������幹��Ϊ�����Σ��ʴ�Ϊ��ǿ��ƽ�������Σ������Σ�
��5���ٵ�һ����������ɵĸ����ӣ������ٽ�һ�������������ɵ������ӣ���H2SeO3��H2SeO4��һ������̶ȴ��ڵڶ������룬
�ʴ�Ϊ����һ����������ɵĸ����ӣ������ٽ�һ�������������ɵ������ӣ�
��H2SeO3��H2SeO4�ɱ�ʾ�ɣ�HO��2SeO�ͣ�HO��2SeO2��H2SeO3�е�SeΪ+4�ۣ���H2SeO4�е�SeΪ+6�ۣ������Ը��ߣ�����Se-O-H��O�ĵ��Ӹ���Seƫ�ƣ�Խ�����H+��H2SeO4��H2SeO3����ǿ��
�ʴ�Ϊ��H2SeO3��H2SeO4�ɱ�ʾ�ɣ�HO��2SeO�ͣ�HO��2SeO2��H2SeO3�е�SeΪ+4�ۣ���H2SeO4�е�SeΪ+6�ۣ������Ը��ߣ�����Se-O-H��O�ĵ��Ӹ���Seƫ�ƣ�Խ�����H+��
��6�������к��а�ɫ��λ�ڶ�������ģ�������8��$\frac{1}{8}$+6��$\frac{1}{2}$=4����ɫ��λ�����ģ���4��������ƽ������4��ZnS������Ϊ4����97��6.02��1023��g�����������Ϊ��540.0��10-10cm��3�����ܶ�Ϊ[4����97��6.02��1023��g]�£�540.0��10-10cm��3=4.1g•cm-3��
bλ�ú�ɫ������Χ4����ɫ����������ṹ����ɫ����������ɫ�����н�Ϊ109��28�䣬aλ�ð�ɫ�������İ�ɫ�����Ϊ540.0pm��$\frac{\sqrt{2}}{2}$=270$\sqrt{2}$pm����aλ��S2-��bλ��Zn2+֮��ľ���Ϊy pm�������������������ߡ��н�������߹�ϵ��y2+y2-2y2cos109��28��=��270$\sqrt{2}$��2�����y=$\frac{270}{\sqrt{1-cos109��28��}}$��
�ʴ�Ϊ��4.1��$\frac{270}{\sqrt{1-cos109��28��}}$��
���� ���⿼�����ʽṹ�����ʣ�Ϊ��Ƶ���㣬�漰�������㡢ԭ���ӻ���ʽ�жϡ�ԭ�Ӻ�������Ų���֪ʶ�㣬���ؿ���ѧ���������㼰�ռ������������ѵ��ǣ�6������㣬��Ŀ�Ѷ��еȣ�


 �ٷ�ѧ����ҵ��������ϵ�д�
�ٷ�ѧ����ҵ��������ϵ�д� ��������ϵ�д�
��������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ֻ�Т� | B�� | �ٺ͢� | C�� | �ٺ͢� | D�� | �٢ڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | pH=1����Һ�У�NH4+��Fe2+��SO42-��Cl- | |
| B�� | ͨ��CO2�������Һ�У�Ca2+��I-��ClO-��NO3-�� | |
| C�� | c��Fe3+��=0.1 mol•L-1����Һ�У�Na+��I-��SCN-��SO42- | |
| D�� | ��ˮ�������c��H+��=1.0��10-13 mol•L-1����Һ�У�Na+��HCO3-��Cl-��Br- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
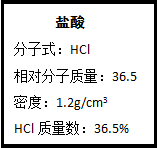 ͼΪʵ����ijŨ�����Լ�ƿ�ϵı�ǩ���Ը����й����ݻش��������⣺
ͼΪʵ����ijŨ�����Լ�ƿ�ϵı�ǩ���Ը����й����ݻش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ʵ����� | ʵ�鲽��Ͳ��� | ʵ������ |
| ʵ��һ | ��I��ȡ������������[�Ѳ��ֱ��ʣ���������������ˮ������Fe��OH��2Cl]�������м������ϡ���ᣮ ��II���ټ����Թ��������ۣ��� | ������ȫ�ܽ⣬��Һ�ʻ���ɫ |
| ʵ��� | ��I��ȡʵ��һ�õ�����Һ������KSCN��Һ�� ��II���ټ�������H2O2��Һ�� | ������ʵ������ ��Һ��죬���������� |
| ʵ���� | ��I��ȡ10mL0.1mol/LKI��Һ���μ�6��0.1mol/L FeCl3��Һ����II��ȡ����������ɫҺ�壬�μ�KSCN��Һ�� ��III����ȡ������ɫҺ�壬���������Һ�� | ��Һ�ʻ�ɫ ��Һ��� ��Һ���� |
| ʵ���� | ��I����ʵ��������I�����õĻ�ɫ��Һ�м���2mLCCl4���������õ�ˮ�㣺�ظ��������Σ� ��II����ʵ���IJ���I������ˮ���м�KSCN��Һ�� | �ϲ���Һ��ɫ �²���ҺΪ��ɫ ������ʵ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��У������ȤС���ڴ�����ˮ��Ʒʱ��������������Ϊ36.5%��Ũ���ᡢ�ܶ�Ϊ1.19g/cm3�����Ƴ�250mL 0.1mol•L-1��������Һ��
��У������ȤС���ڴ�����ˮ��Ʒʱ��������������Ϊ36.5%��Ũ���ᡢ�ܶ�Ϊ1.19g/cm3�����Ƴ�250mL 0.1mol•L-1��������Һ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
�� ��B�ĽṹʽΪ
��B�ĽṹʽΪ ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ۢ� | B�� | �٢ܢ� | C�� | �ڢۢ� | D�� | �ۢܢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com