

| 1.92g |
| 64g/mol |
| 0.224L |
| 22.4L/mol |
| 0.01mol×4 |
| 2 |
| 4.8g |
| 160g/mol |
| ||
| ||


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
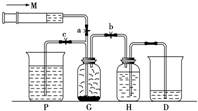 某课外活动小组利用如图所示的装置制取Cl2,提供的试剂有浓盐酸、饱和食盐水(Cl2在其中溶解度较小)、氢氧化钠溶液、高锰酸钾固体,反应的化学方程式为:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
某课外活动小组利用如图所示的装置制取Cl2,提供的试剂有浓盐酸、饱和食盐水(Cl2在其中溶解度较小)、氢氧化钠溶液、高锰酸钾固体,反应的化学方程式为:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O查看答案和解析>>
科目:高中化学 来源: 题型:
| A、M中没有甲基? |
| B、A的属于酯的同分异构体还有一种 |
| C、N、M均不能发生银镜反应 |
| D、N分子中含有甲基? |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
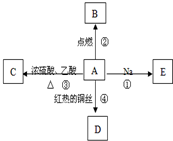 A是化学实验室中最常见的有机物,它易溶于水并有特殊香味,并能进行如图所示的多种反应.B物质中含有碳元素.
A是化学实验室中最常见的有机物,它易溶于水并有特殊香味,并能进行如图所示的多种反应.B物质中含有碳元素.查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

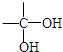
| 自动脱水 |


| 醇 |
| 浓H2SO4/△④ |

| 催化剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com