
分析 硫在空气燃烧生成A,A是SO2;SO2是酸性氧化物,能和水反应生成 B为 H2SO3;H2SO3 具有还原性,I2具有氧化性,H2SO3和I2能发生氧化还原反应得H2SO4 和 HI,HI具有还原性,Na2S具有还原性,所以HI和Na2S不能发生氧化还原反应,C能与Na2S反应,所以C是H2SO4、D是HI,C与Na2S反应得到含硫化合物E为 H2S,所以A是SO2、B 是H2SO3、C是H2SO4、D是HI、E 是H2S,据此答题.
解答 解:硫在空气燃烧生成A,A是SO2;SO2是酸性氧化物,能和水反应生成 B为 H2SO3;H2SO3 具有还原性,I2具有氧化性,H2SO3和I2能发生氧化还原反应得H2SO4 和 HI,HI具有还原性,Na2S具有还原性,所以HI和Na2S不能发生氧化还原反应,C能与Na2S反应,所以C是H2SO4、D是HI,C与Na2S反应得到含硫化合物E为 H2S,所以A是SO2、B 是H2SO3、C是H2SO4、D是HI、E 是H2S,
(1)根据上面的分析可知,B 是H2SO3,D是HI,
故答案为:H2SO3;HI;
(2)E 是H2S具有还原性,SO2既有氧化性又有还原性,H2S能和SO2发生氧化还原反应,方程式为:2H2S+SO2=3S+2H2O,
故答案为:2H2S+SO2=3S+2H2O.
点评 本题考查了硫元素及其化合物的性质,侧重于考查学生对基础知识的综合应用能力,注意把握各物质的相互转化,题目难度不大.


 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 2X2+3Y2?2X2Y3 | B. | 3X2+2Y2?2X3Y2 | C. | X2+2Y2?XY2 | D. | 2X2+Y2?2X2Y |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 饱和Na2SO4溶液可以使蛋白质变性 | |
| B. | 大力推广应用“脱硫、脱硝”技术,可减少硫氧化物、氮氧化物对空气的污染 | |
| C. | 从海带中提取碘单质的过程涉及氧化还原反应 | |
| D. | 镀锌铁桶镀层破损后铁仍不易被腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向Mg(HCO3)2溶液中加入过量的NaOH溶液Mg2++2HCO3-+2OH-═MgCO3↓+CO32-+2H2O | |
| B. | 溴化亚铁溶液中通入足量的氯气:2Fe2++Cl2═2Fe3++2Cl- | |
| C. | 少量的CO2通入稀的碳酸钠溶液中:CO2+CO32-+H2O═2HCO3- | |
| D. | 向NH4Al(SO4)2溶液中滴入Ba(OH)2使SO42-反应完全2Ba2++4OH-+Al3++2SO42-═2BaSO4↓+AlO2-+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应A(g)?2B(g)△H,若正反应的活化能为Ea kJ•mol-1,逆反应的活化能为Eb kJ•mol-1,则△H=-(Ea-Eb)kJ•mol-1 | |
| B. | 某温度下,氯化钠在水中的溶解度是20g,则该温度下的饱和氯化钠溶液溶质的质量分数为20% | |
| C. | 将浓度为0.1 mol•L-1HF溶液加水不断稀释过程中,电离平衡常数Ka(HF)保持不变,$\frac{{c({F^-})}}{{c({H^+})}}$始终保持增大 | |
| D. | 将0.2 mol•L-1的CH3COOH溶液与0.1 mol•L-1的NaOH溶液等体积混合后,溶液中有关粒子的浓度满足下列关系:2c(H+)-2c(OH-)=c(CH3COO-)-c(CH3COOH) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
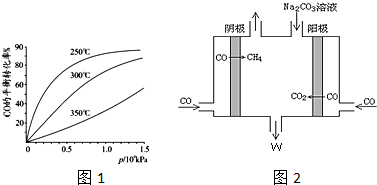
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子半径:Q>W>Z | |
| B. | Q的氢化物的水溶液一定具有强酸性 | |
| C. | X、Y、Q可同时存在同一离子化合物中 | |
| D. | 单质的沸点:W>Q>Z |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com