
| A. | 1.8gH2O与CH2D2的混合物中所含质子数为NA | |
| B. | 1mol甲烷或白磷(P4)分子中所含共价键数均为4NA | |
| C. | 1mol CH3COOC2H5在稀硫酸溶液中水解可得到乙醇分子数为NA | |
| D. | 25℃时,l L pH=1的H2SO4溶液中含有的H+ 数为0.2NA |
分析 A.H2O与CH2D2的相对分子质量为都是18,质子数都是10个;
B.1个甲烷分子含有4个C-H键,1个白磷分子含有6个P-P键;
C.酯的水解反应为可逆反应,不能进行到底;
D.pH=1的H2SO4溶液氢离子浓度为0.1mol/L,依据n=CV计算解答;
解答 解:A.1.8gH2O与CH2D2的物质的量为$\frac{1.8g}{18g/mol}$=0.1mol,含有质子数为0.1mol×NA=NA,故A正确;
B.1mol甲烷含共价键数均为4NA,1mol白磷(P4)分子中所含共价键数均为6NA,故B错误;
C.酯的水解反应为可逆反应,不能进行到底,所以1mol CH3COOC2H5在稀硫酸溶液中水解可得到乙醇分子数小于NA,故C错误;
D.pH=1的H2SO4溶液氢离子浓度为0.1mol/L,25℃时,l L pH=1的H2SO4溶液中含有的H+ 数为0.1mol×1L×NA=0.1NA,故D错误;
故选:A.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,注意可逆反应特点、题目难度不大.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
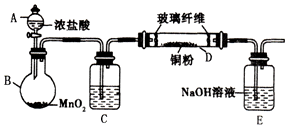 实验室采用如图所示的装置制取氯化铜(部分仪器和夹持装置已略去).
实验室采用如图所示的装置制取氯化铜(部分仪器和夹持装置已略去).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯与液溴FeBr3作催化剂的条件下发生取代反应,生成溴苯 | |
| B. | 分子式为C5H10Q2,且能与NaHCO3反应的有机物有3种 | |
| C. | 乙醇制备乙烯和乙醇制备乙酸乙酯均为取代反应 | |
| D. | 2-甲基戊烷和4-甲基戊烷互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 法国、美国、荷兰的三位科学家因研究“分子机器的设计与合成”获得2016年诺贝尔化学奖.轮烷是一种分子机器的“轮子”,合成轮烷的基本原料有CH2C12、丙烯、戊醇、苯,下列说法不正确的是( )
法国、美国、荷兰的三位科学家因研究“分子机器的设计与合成”获得2016年诺贝尔化学奖.轮烷是一种分子机器的“轮子”,合成轮烷的基本原料有CH2C12、丙烯、戊醇、苯,下列说法不正确的是( )| A. | CH2C12有两种同分异构体 | |
| B. | 丙烯能使溴水褪色 | |
| C. | 戊醇在一定条件下能与乙酸发生酯化反应 | |
| D. | 苯与足量氢气在镍催化作用下会发生加成反应生成环己烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
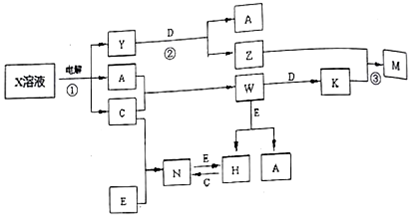
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com