
下列有关实验操作、现象和解释或结论都正确的是
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 过量的Fe粉中加入稀HNO3,充分反应后,滴入KSCN溶液 | 溶液呈红色 | 稀HNO3将Fe氧化为Fe3+ |
| B | AgI沉淀中滴入稀KCl溶液 | 有白色沉淀出现 | AgCl比AgI更难溶 |
| C | Al箔插入稀HNO3中 | 无现象 | Al箔表面被HNO3氧化,形成致密的氧化膜 |
| D | 用玻璃棒蘸取浓氨水点到红色石蕊试纸上 | 试纸变蓝色 | 浓氨水呈碱性 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
下列除杂方案错误的是
| 选项 | 被提纯的物质 | 杂质 | 除杂试剂 | 除杂方法 |
| A | CO(g) | CO2(g) | NaOH 溶液、浓 H2SO4 | 洗气 |
| B | NH4Cl(aq) | Fe3+(aq) | NaOH溶液 | 过滤 |
| C | Cl2(g) | HCl(g) | 饱和食盐水、浓H2SO4 | 洗气 |
| D | Na2CO3(s) | NaHCO3(s) | — | 灼烧 |
查看答案和解析>>
科目:高中化学 来源: 题型:
氮的氧化物对人体危害极大,实验时应防止其对空气的污染。
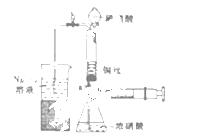 实验一:某同学利用下列装置实
实验一:某同学利用下列装置实 现铜与浓硝酸、稀硝酸的反应。
现铜与浓硝酸、稀硝酸的反应。
Ⅰ、取一段铜丝,用稀硫酸除去铜锈[主要成分是Cu2(OH)2CO3]。
Ⅱ、将洗涤后的铜丝做成匝数较多的螺旋状。
Ⅲ、按如图所示装置连接仪器、检查气密性、装入化学试剂。
(1)请完成过程Ⅰ发生反应的离子方程式:Cu2(OH)2CO3+4H+= 。
(2)过程Ⅲ的后续操作如下:
① 为使浓硝酸与铜丝接触,操作是打开止水夹a和b, ,当红棕色气体较多时,轻抽注射器使反应停止,关闭a,取下注射器。
生成红棕色气体的化学方程式是 。
② 控制b与分液漏斗活塞,玻璃管充满稀硝酸时, 关闭b打开a,可见有无色气体产生。
关闭b打开a,可见有无色气体产生。
稀硝酸充满玻璃管的目的是 。
实验二:NO2与水反应的实验研究。
(3)将3支充满红棕色气体的小试管分倒置在盛有常温水、热水和冰水的3只烧杯中,发现液面上升的高度明显不一致。结果如下表所示(忽略温度对气体体积的影响):

① 根据上表得出的结论是温度越 (填“高”或“低“),进入试管中的溶液越多。
② 查阅材料:a.NO2与水反应的实际过程为:2NO2+ H2O=HNO3+ HNO2,3 HNO2= HNO3+2NO↑+H2O;b. HNO2不稳定。则产生上述现象的原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下,浓度都是1 mol/L的两种气体X2和Y2,在密闭容器中反应生成气体Z,经过t min后,测得
各物质的浓度分别 为c(X2)=0.4 mol/L,c(Y2)=0.6 mol/L,c(Z)=0.4 mol/L,则该反应的化学方程式可表示为 ( )
为c(X2)=0.4 mol/L,c(Y2)=0.6 mol/L,c(Z)=0.4 mol/L,则该反应的化学方程式可表示为 ( )
A.2X2+3Y2 2X2Y3 B.3X2+2Y2
2X2Y3 B.3X2+2Y2 2X3Y2
2X3Y2
C.X2+2Y2 2XY2 D.2X2+Y2
2XY2 D.2X2+Y2 2X2Y
2X2Y
查看答案和解析>>
科目:高中化学 来源: 题型:
在C(s)+CO2(g)2CO(g)反应中,可使反应速率增大的措施是 ( )
①增 大压强 ②增加炭的量 ③通入CO2 ④恒压下充入N2 ⑤恒容下充入N2 ⑥通入CO
大压强 ②增加炭的量 ③通入CO2 ④恒压下充入N2 ⑤恒容下充入N2 ⑥通入CO
A.①③④ B.②④⑥
C.①③⑥ D.③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
某研究性学习小组查阅资料知:O2在酸性环境中氧化性明显增强,为了探究过氧化钠的强氧化性,设计了如图的实验装置。实验步骤及现象如下:
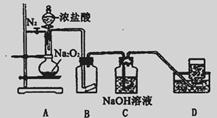
①检查装置气密性后,装入药品并连接仪器:
②缓慢通入一定量的N2后,将装置D连接好(导管末端未伸入集气瓶中),再向圆底烧瓶中缓慢滴加浓盐酸,剧烈反应,产生黄绿色气体。
③一段时间后,将导管末端伸入集气瓶中收集气体。装置D中收集到能使带火星的木条复燃的无色气体。
④反应结束后,关闭分液漏斗的活塞,再通入一定量N2,至装置中气体无色。回答下列问题:
(1)装置B中的湿润的红色纸条褪色,证明A中反应有__________(填化学式)生成。
若B中改放湿润的淀粉KI试纸,仅凭试纸变蓝的现象不能证明上述结论,请用离子方程式说明原因__________________________。
(2)装置C的作用是_________________________________。
(3)甲同学认为O2是Na2O2被盐酸中的HCl还原所得。乙同学认为此结论不正确,他可能的理由为①O2有可能是Na2O2与盐酸中的H2O反应所得:②___________________。
(4)实验证明,Na2O2与干燥的HC1能反应,该反应_______________(填“能”或“不能”)用于实验室快速制取纯净的C12,理由是(要求从两个不同的方面答出要点)
①_____________________;②_________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
SiO2、SO2和CO2都是酸性氧化物,它们的化学性质有一定的相似性;Mg和Na的化学性质也有一定相似性。某兴趣小组用如图所示装置进行Mg与SO2反应的实验。
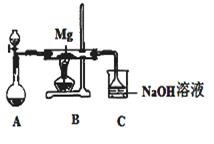
(1)选择制取SO2的合适试剂 (填编号)。
①浓HCl ②浓H2SO4
③Na2SO3固体 ④CaSO3固体
(2)上述装置还可改进,改进的方法是
,
若C中NaOH为0.2mol/L、200ml,通入的SO2为1.12L(标准状况),则该反应的离子方程式为
(3)甲同学推测Mg与SO2的反应与CO2相似,则该反应方程式为
乙同学的推测是:2Mg+3SO2 2MgSO3+S;
2MgSO3+S;
丙同学的推测是:3Mg+SO2 2MgO+MgS,
2MgO+MgS,
要验证甲、乙、丙三位同学的推测是否正确,丁同学作如下实验探究:
已知:MgSO3和MgS都是微溶于水,能与盐酸发生复分解反应放出气体;
限选试剂:2mol/L HCl、2mol/L HNO3、蒸馏水、2mol/L NaOH、品红溶液、澄清石灰水、2mol/L CuSO4;仪器和用品自选。请填写下表中的空格:
根据上述实验探究:
| 序号 | 实验步骤 | 预期现象和结论 |
| ① | 取少量反应后的固体于试管I中 |
|
| ② | 向试管I中的固体慢慢滴加 试管I口塞上带导管的单孔塞,并将导管通入盛有 的试管II中。 | 若试管I中的 , 则丙同学推测正确。若试管I中的固体未完全溶解,且 ,则乙同学的推测正确。 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是 ( )
A.正常雨水的pH为7.0,酸雨的pH小于7.0
B.可使用二氧化硫和某些含硫化合物对食品进行增白
C.使用氯气对自来水消毒过程中,生成的有机氯化物可能对人体有害
D.食品厂产生的含丰富氮、磷的废水可长期排向水库养鱼
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学为了验证海带中含有碘元素,拟进行如下实验,请完成相关问题。
(1)第1步:灼烧。操作是将足量海带灼烧成灰烬。该过程中不会用到的实验仪器有 (填代号)。
A.试管 B.瓷坩埚 C.坩埚钳 D.铁三脚架
E.泥三角 F.酒精灯 G.烧杯 H.量筒
(2)第2步:I-溶液的获取。操作是 。
(3)第3步:氧化。操作是依次加入合适的试剂。下列氧化剂最好选用 (填代号)。
A.浓硫酸 B.新制氯水
C.KMnO4溶液 D.H2O2
理由是 。
(4)第4步:碘单质的检验。操作是取少量第3步的溶液,滴加淀粉溶液,如果溶液显蓝色,则证明海带中含有碘元素。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com