


科目:高中化学 来源:不详 题型:计算题
| 实验序号 | 样品的质量/g | NaOH溶液的体积/mL | 氨气的体积/L |
| 1 | 3.62 | 50.00 | 0.896 |
| 2 | 7.24 | 50.00 | 1.792 |
| 3 | 10.86 | 50.00 | 2.016 |
| 4 | 14.48 | 50.00 | 1.568 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
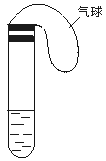
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.2.24 L气体的质量一定小于或等于3.4 g | B.原混合物中一定含有5.6 gFe | C.原混合物的质量不可能大于8.8 g | D.原混合物加热反应后的物质肯定是纯净物 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
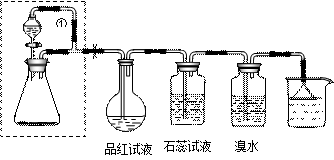
 ①能使澄清石灰水变浑浊 ②能使湿润的蓝色石蕊试纸变红 ③能使品红试液褪色,加热后又显红色 ④能使溴水褪色,再滴加酸化的BaCl2溶液有白色沉淀产生
①能使澄清石灰水变浑浊 ②能使湿润的蓝色石蕊试纸变红 ③能使品红试液褪色,加热后又显红色 ④能使溴水褪色,再滴加酸化的BaCl2溶液有白色沉淀产生
| A.①②③④ | B.①③④ | C.③④ | D.②③④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.SO2不能用来漂白食品 |
| B.SO2具有漂白性,可以使品红溶液褪色 |
| C.SO2与水反应生成H2SO4 |
| D.SO2是一种大气污染物,它主要来自于化石燃料的燃烧 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.大理石(主要成分为CaCO3)墙面 |
| B.竹、木房屋 |
| C.铜铸塑像 |
| D.塑胶跑道 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com