
| A. | 46g乙醇中含极性键数目为8NA | |
| B. | 2H2S+SO2=3S↓+2H2O中消耗1mol还原剂时转移电子数为4NA | |
| C. | 向1L1mol•L-1CH3COOH溶液中加入足量的铁粉充分反应,产生的氢分子数为0.5NA | |
| D. | 在6CO2+12H218O=C6H12O6+618O2+6H2O中,每产生13.44L氧气(标准状况),净减水分子数为1.2NA |
分析 A、乙醇中含有的6条C-H键和1条C-O键为极性键;
B、反应2H2S+SO2=3S↓+2H2O转移4mol电子,消耗还原剂H2S2mol;
C、求出醋酸的物质的量,然后根据铁和醋酸反应时,2molH+~1mol氢气来分析;
D、在6CO2+12H218O=C6H12O6+618O2+6H2O中,当生成6mol氧气时,净消耗6mol水.
解答 解:A、乙醇中含有的6条C-H键和1条C-O键为极性键,故46g乙醇即1mol乙醇中含7NA条极性键,故A错误;
B、反应2H2S+SO2=3S↓+2H2O转移4mol电子,消耗还原剂H2S2mol,故当消耗1mol还原剂时转移2NA个电子,故B错误;
C、溶液中醋酸的物质的量n=CV=1mol/L×1L=1mol,而铁和醋酸反应时,2molH+~1mol氢气,故1mol醋酸生成0.5mol氢气即0.5NA个氢气分子,故C正确;
D、在6CO2+12H218O=C6H12O6+618O2+6H2O中,当生成6mol氧气时,净消耗6mol水,故当生成13.44L氧气即0.6mol氧气时,则净消耗0.6mol水即0.6NA个水分子,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.


 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:选择题
| A. | 由于氢键的作用,使NH3、H2O、HF的沸点反常,且沸点高低顺序为HF>H2O>NH3 | |
| B. | 氢键只能存在于分子间,不能存在于分子内 | |
| C. | 在固态水(冰)中,水分子间氢键数目增多,造成体积膨胀,密度减小,水的这种性质对水生生物的生存有重要意义 | |
| D. | 相同量的水在气态、液态和固态时均有氢键,且氢键的数目依次增多 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;结构式⑥O=C=O.
;结构式⑥O=C=O. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 符合通式CnH2n+2(n≥1)且相对分子质量不相等的有机物为同系物 | |
| B. | 符合同一通式且相对分子质量不相等的有机物为同系物 | |
| C. | 乙醇和甲醚不是同系物但是同分异构体 | |
| D. | CH3CH2CHO、CH2═CHCH2OH、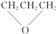 三种物质互为同分异构体 三种物质互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
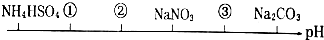
| A. | NH4Cl (NH4)2SO4 CH3COONa | B. | (NH4)2SO4 NH4Cl CH3COONa | ||
| C. | (NH4)2SO4 NH4Cl NaOH | D. | CH3COOH NH4Cl (NH4)2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
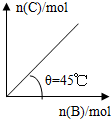
| A. | 平衡时B的转化率为40% | |
| B. | 若再通入B,则再次达平衡时C的体积分数增大 | |
| C. | 在容器中加入催化剂,则B的转化率增大 | |
| D. | 若保持压强一定,当温度升高时,图中θ>45° |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ②③ | C. | ③④ | D. | ①④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com