
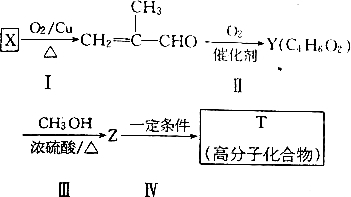
 ,据此答题.
,据此答题. ,
,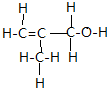 ,故答案为:
,故答案为: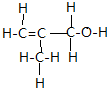 ;
;| 一定条件 |
 ,故答案为:nCH2=C(CH3)COOCH3
,故答案为:nCH2=C(CH3)COOCH3| 一定条件 |
 ;
; ,故答案为:
,故答案为: ;
;

科目:高中化学 来源: 题型:
| A、pH=1的溶液中:Na+、Mg2+、SO42-、HCO3- |
| B、含有大量Fe3+的溶液中:.Al3+、Cu2+、Cl-、SO42- |
| C、加入Al能放出H2的溶液中:K+、NH4+、NO3-、Cl- |
| D、使蓝色石蕊试纸变红的溶液:K+、S2-、NO3-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
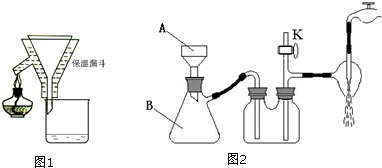
A、 制取并收集乙炔 |
B、 比较NaHCO3、Na2HCO3的热稳定性 |
C、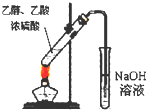 实验室中制取少量乙酸乙酯 |
D、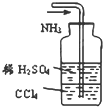 吸收多余的NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| NaNO3 | KNO3 | NaCl | KCl | |
| 10°C | 80.5 | 20.9 | 35.7 | 31.0 |
| 100°C | 175 | 246 | 39.1 | 56.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③ | B、②③ | C、①④ | D、②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
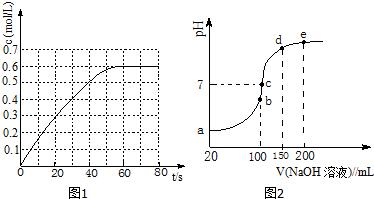
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③ | B、①④ | C、③④ | D、①② |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com