
下列叙述正确的是 ( )
A.将稀氨水逐滴加入稀硫酸中,当溶液pH=7时,c(SO42-)>c(NH4+)
B.两种醋酸溶液的物质的量浓度分别为c1和c2,pH分别为a和a+1,则c1=10c2
C.pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴入石蕊溶液呈红色
D.向0.1 mol/L的氨水中加入少量硫酸铵固体,则溶液中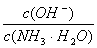 增大
增大
科目:高中化学 来源: 题型:
下列各项叙述中,正确的是( )。
A.镁原子由 1s22s22p63s2→1s22s22p63p2 时,原子释放能量,由基态转化成激发态
B.价电子排布为 5s25p1 的元素位于第五周期第ⅠA 族,是 s 区元素
C.所有原子任一能层的 s 电子云轮廓图都是球形,但球的半径大小不同
D.24Cr 原子的电子排布式是1s22s22p63s23p63d44s2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子因发生氧化还原反应而不能大量共存的是 ( )
A.H+、Fe2+、Cr2O72-、SO42- B.Ca2+、H+、SO42-、HCO3-
C.Na+、Cu2+、Cl-、S2- D.Fe3+、K+、SCN-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
某学生设计了一个“黑笔写红字”的趣味实验。滤纸先用氯化钠、无色酚酞的混合液浸湿,然后平铺在一块铂片上,接通电源后,用铅笔在滤纸上写字,会出现红色字迹。据此,下列叙述正确的是 ( )
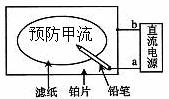
A.铅笔端作阳极,发生还原反应 B.铂片端作阴极,发生氧化反应
C.铅笔端有少量的氯气产生 D.a点是负极,b点是正极
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子能在指定溶液中共存的是 ( )
①无色溶液中: 、
、 、
、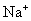 、
、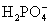 、
、 、
、
②使pH试纸变深蓝的溶液中: 、
、 、
、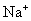 、
、 、
、 、
、
③水电离的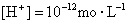 的溶液中:
的溶液中: 、
、 、
、 、
、 、
、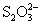
④加入Mg能放出 的溶液中:
的溶液中: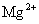 、
、 、
、 、
、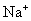 、
、
⑤使甲基橙变红的溶液中: 、
、 、
、 、
、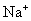 、
、
⑥pH=0的溶液中: 、
、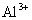 、
、 、
、 、
、 、
、
A.①③ B.②④⑤ C.①②⑤ D.③⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关物质性质的应用错误的是
A.二氧化硅不与强酸反应,可用石英玻璃容器盛放氢氟酸
B.碳酸氢钠具有弱酸性,可用于食品发酵
C.次氯酸钠具有强氧化性,可用于配制消毒液
D.明矾能水解生成Al(OH)3胶体,可用作净水剂
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关说法正确的是
A.钢铁的腐蚀过程中,析氢腐蚀与吸氧腐蚀不可能同时发生
B.反应NH4Cl(s)=NH3(g)+HCl(g)在室温下不能自发进行,则该反应的ΔH>0
C.由于Ksp(BaSO4)<Ksp(BaCO3),因此BaSO4沉淀不可能转化为BaCO3 沉淀
D.25℃时,0.1 mol·L-1CH3COOH溶液加水稀释后,c(OH-)/c(CH3COOH)增大
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关电解质溶液的说法正确的是( )
A.将Ca(ClO)2、Na2SO3、FeCl3溶液蒸干均得不到原溶质
B.保存氯化亚铁溶液时,在溶液中放少量铁粉,以防止Fe2+水解
C.室温下,向0.1mol/L的CH3COOH溶液中加入少量水溶液显碱性的物质,CH3COOH的电离程度一定增大
D.NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同
查看答案和解析>>
科目:高中化学 来源: 题型:
原子序数依次增大的X、Y、Z、G、Q、R、T七种元素,核电荷数均小于36。已知X的一种1:2型氢化物分子中既有σ键又有π键,且所有原子共平面;Z的L层上有2个未成对电子;Q原子的s能级与p能级电子数相等;R单质是制造各种计算机、微电子产品的核心材料;T处于周期表的ds区,原子中只有一个未成对电子。
(1)Y原子核外共有________种不同运动状态的电子,T原子有________种不同能级的电子。
(2)X、Y、Z的第一电离能由小到大的顺序为________(用元素符号表示)。
(3)由X、Y、Z形成的离子ZXY-与XZ2互为等电子体,则ZXY-中X原子的杂化轨道类型为________。
(4)Z与R能形成化合物甲,1 mol甲中含________ mol化学键,甲与氢氟酸反应,生成物的分子空间构型分别为________。
(5)G、Q、R氟化物的熔点如下表,造成熔点差异的原因为_________________
________________________________________________________。
| 氟化物 | G的氟化物 | Q的氟化物 | R的氟化物 |
| 熔点/K | 993 | 1 539 | 183 |
(6)向T的硫酸盐溶液中逐滴加入Y的氢化物的水溶液至过量,反应的离子方程式为__________________________。
(7)X单质的晶胞如图所示,一个X晶胞中有________个X原子;若X晶体的密度为ρ g·cm-3,阿伏加德罗常数的值为NA,则晶体中最近的两个X原子之间的距离为________ cm(用代数式表示)。
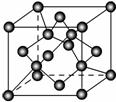
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com